Madame, Monsieur,
L’infortune d’un désir de grossesse non satisfait n’est pas rare. Dans les pays industrialisés, 12-15% des couples n’arrivent pas à concevoir après un an d’activité sexuelle régulière. Si une information précise et quelques mesures simples peuvent apporter une grande aide à courte échéance, il faut savoir que dans bien des cas, des investigations spécifiques et des thérapies complexes doivent être proposées, afin de tenter l’obtention d’une grossesse.
Depuis 2005 le Centre Hospitalier du Luxembourg est fier d’accueillir le Laboratoire National de Procréation Médicalement Assistée (PMA). Notre service dispose des moyens diagnostics et thérapeutiques pour prendre en charge le couple infertile. Ainsi, les médecins spécialisés en médecine de reproduction vous prennent en charge en étroite collaboration avec votre gynécologue habituel.
À l’aide de ce dossier-guide nous aimerions vous faciliter le premier contact avec la médecine de reproduction et vous guider dans le cheminement dans notre centre. Nous souhaitons rendre votre vécu du traitement avec ses différentes étapes le plus acceptable possible, que ce soit sur le plan physique, psychologique, médical, social ou encore professionnel.
Prenez le temps de lire attentivement ces quelques pages et n’hésitez pas à poser vos questions à l’équipe de PMA. Nous vous souhaitons un succès rapide.
A bientôt, l’équipe de PMA
Connaissances théoriques de la fertilité
La reproduction chez l'homme
Contrairement à la femme, chez laquelle on note une accélération importante dans l’épuisement du stock folliculaire à partir de l’âge de 37 ans, chez l’homme la spermatogenèse se déroule depuis la puberté jusqu’à un âge plus avancé. Les spermatozoïdes se développent dans les testicules à partir des cellules germinales de réserve. Cette production de spermatozoïdes a lieu dans la paroi des tubes séminifères, des tubes pelotonnés (environ 500 par testicule) qui communiquent ensuite avec l’épididyme. Celui-ci est constitué d’un très fin canalicule d’environ 5 mètres de long. Au cours de la traversée de ce canalicule, les spermatozoïdes terminent leur maturation, en attendant d’être éjaculés.
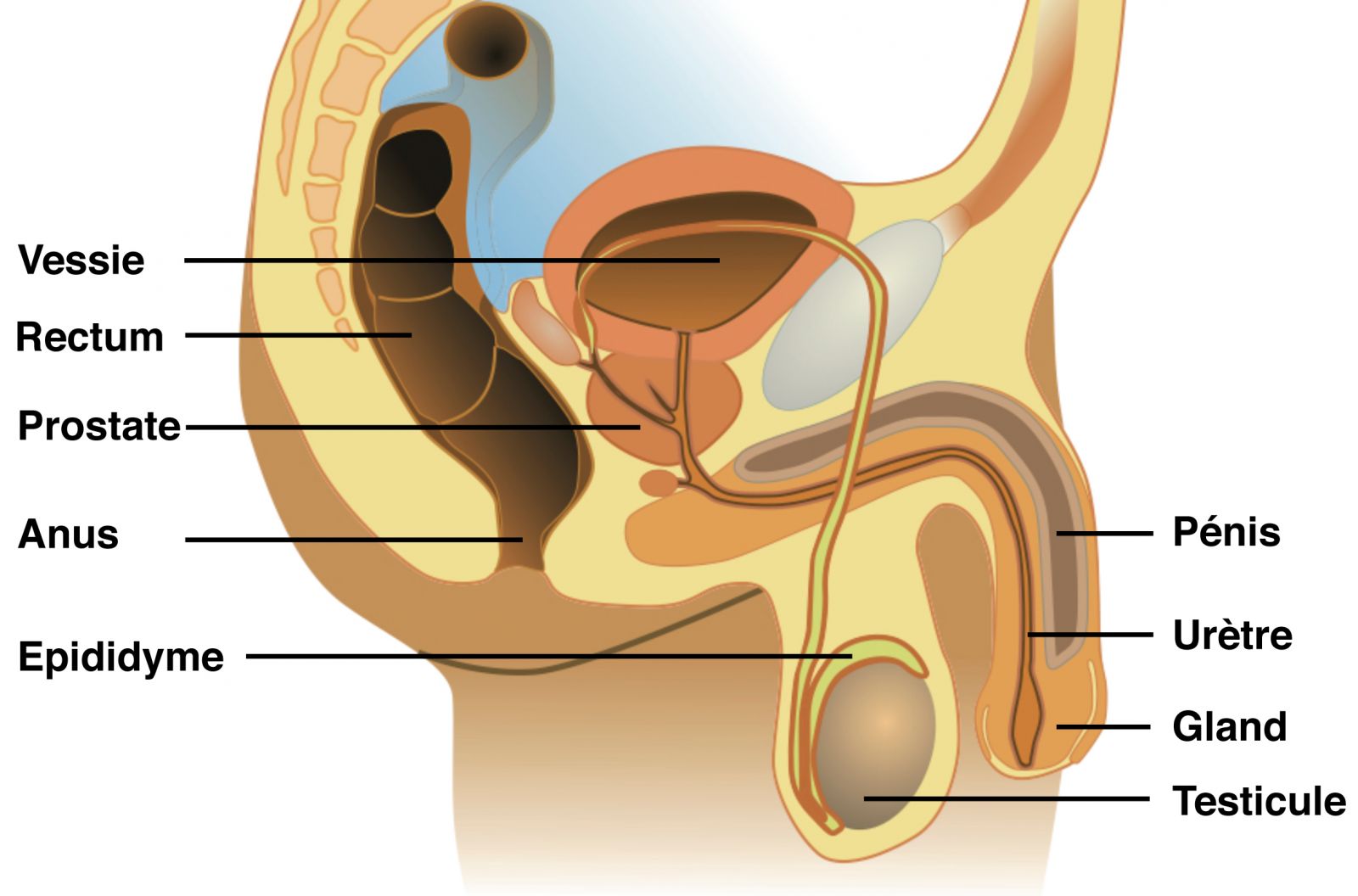
Au moment de l’éjaculation, les spermatozoïdes sont expulsés à travers les 2 canaux déférents qui remontent dans le pelvis, et s’unissent avec les canaux excréteurs des vésicules séminales pour former les canaux éjaculateurs. Ceux-ci traversent la prostate et se jettent dans l’urètre qui s’ouvre au niveau du gland du pénis.
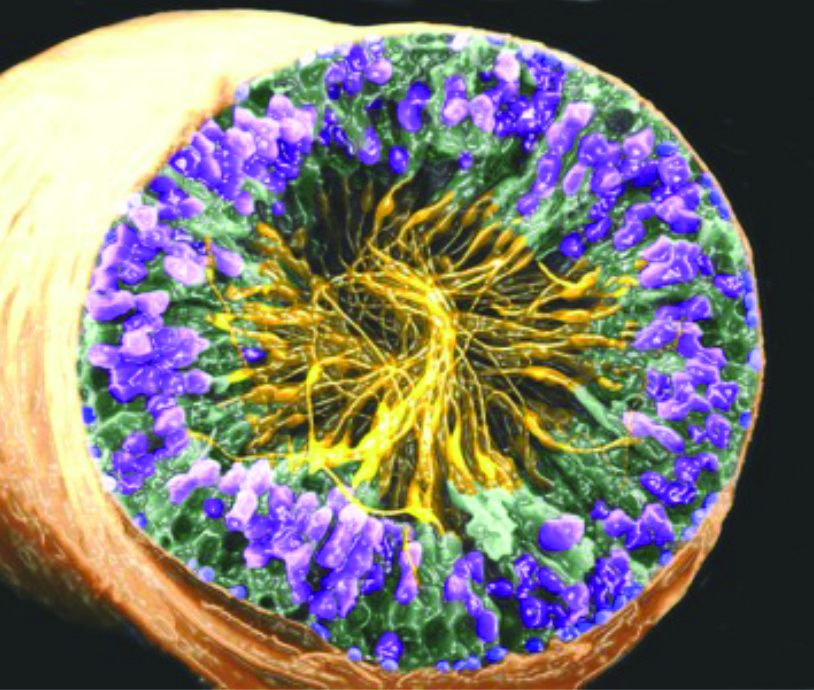
Tube séminifère
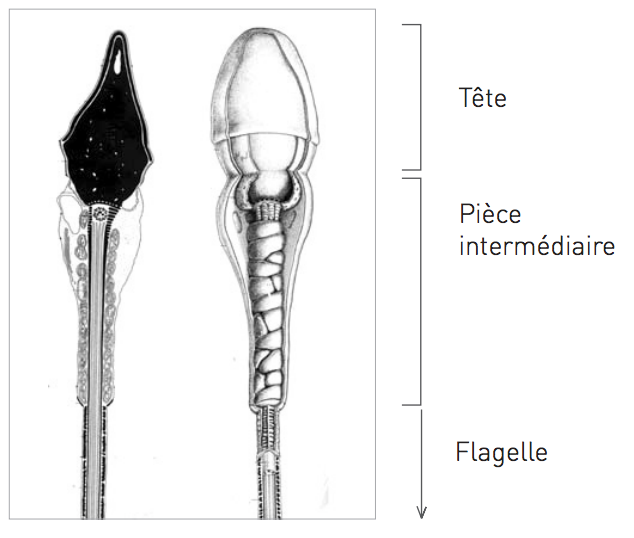
On peut distinguer 3 parties au niveau du spermatozoïde :
- la tête (4 µm) avec le noyau (contenant le matériel génétique) et l’acrosome (un capuchon contenant des enzymes nécessaires pour franchir les enveloppes de l’ovocyte
- la pièce intermédiaire (5 µm) qui fournit l’énergie pour le mouvement.
La reproduction chez la femme
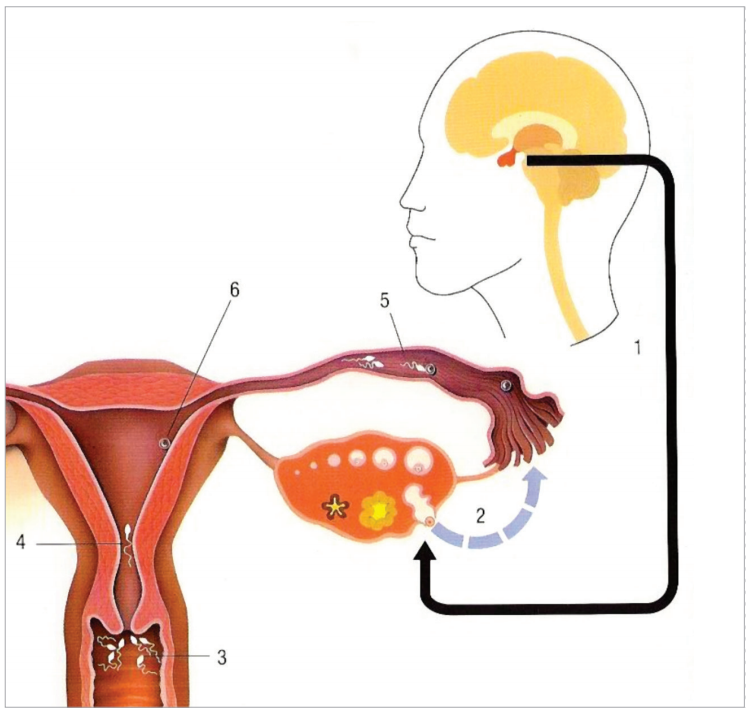
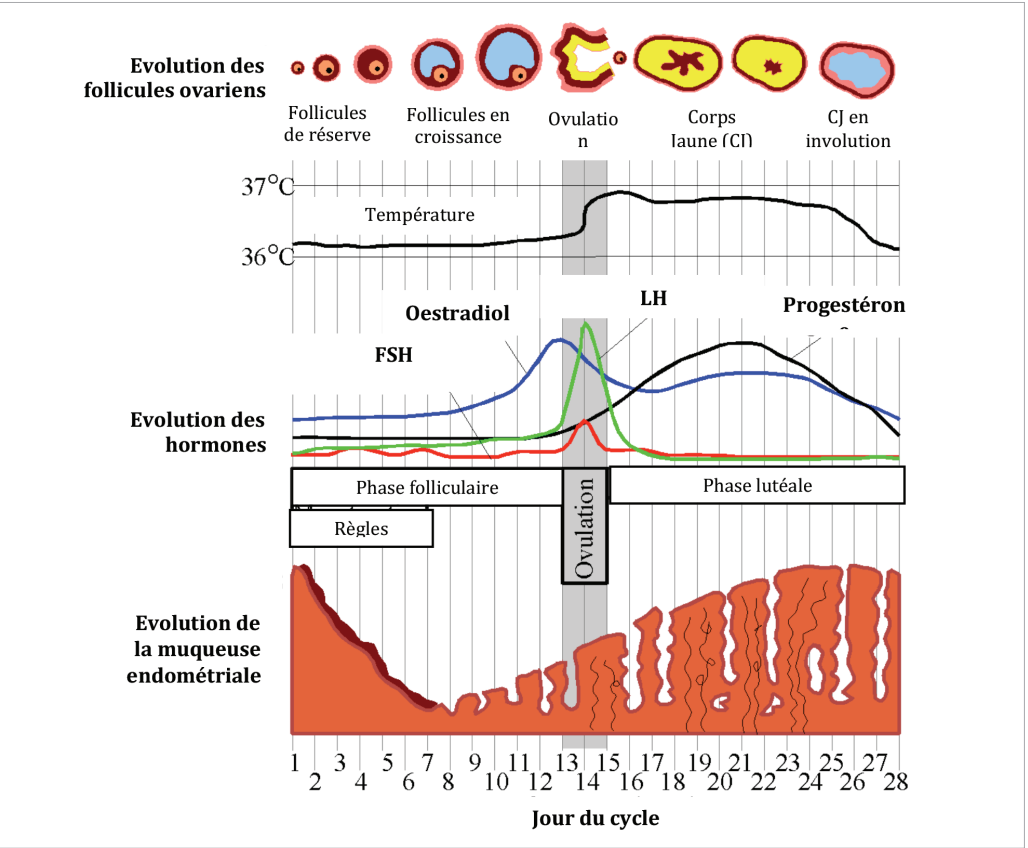
Au début de chaque cycle, l’hypophyse, une glande située à la base du cerveau, sécrète dans le sang une hormone appelée FSH (follicle-stimulating hormone), afin de stimuler la croissance d’un groupe de follicules au niveau des ovaires (figure 4). Le follicule est un petit sac rempli d’un liquide transparent, le liquide folliculaire, dans lequel baigne un ovocyte, une grande cellule de l’ordre du dixième de millimètre.
A la naissance, les ovaires possèdent leur stock dé- finitif de follicules. Ce capital folliculaire diminue ensuite tout au long de la vie par le fait que des follicules quittent la réserve ovarienne pour entamer leur croissance. Ainsi, on peut généralement visualiser par échographie en début de chaque cycle, dans chaque ovaire, entre 5 et 12 follicules en croissance, mesurant entre 2 et 6 mm. Dans un cycle naturel, donc non stimulé par des médicaments, un phénomène de sélection fait qu’après quelques jours, un seul follicule va pouvoir continuer sa croissance, les follicules restants arrêteront leur développement et disparaîtront.
Les follicules sécrètent de l’œstradiol, le taux variant en fonction de la taille et du nombre des follicules. Lorsque le taux d’œstradiol est suffisant et que le follicule sélectionné a atteint une taille de 18-20 mm, l’hypophyse déclenche la libération de l’ovocyte contenu dans ce follicule en sécrétant une deuxième hormone, la LH (luteinizing hormone, figure 6). En effet l’ovulation a lieu environ 36 heures après le pic de LH.
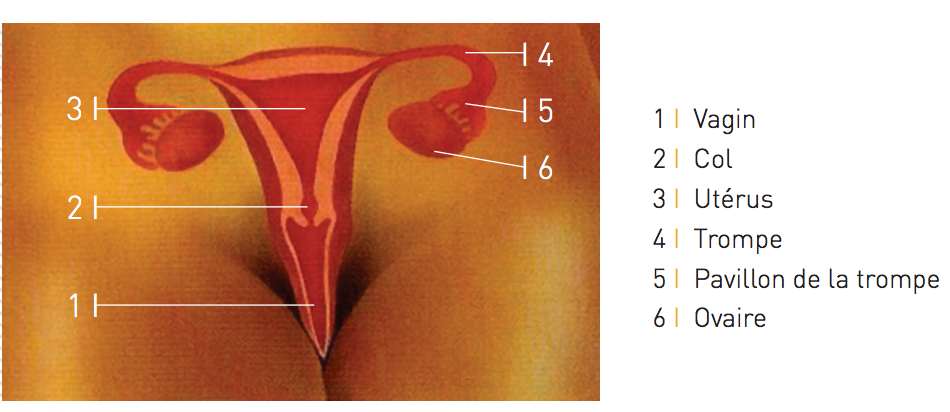
L’ovocyte ainsi libéré est aspiré par le pavillon et transporté dans l’ampoule de la trompe où se fait la rencontre avec le spermatozoïde.
L’embryon qui résulte de la fécondation de l’ovocyte par le spermatozoïde, migre dans l’utérus à travers la trompe, tout en subissant des divisions cellulaires successives, et s’accroche dans l’endomètre qui tapisse l’intérieur de l’utérus. Ce phénomène d’implantation se produit 6 jours après l’ovulation.
Au niveau de l’ovaire, le follicule vidé de son ovocyte, se transforme en corps jaune lequel secrète de l’œstradiol, mais aussi de la progestérone, l’hormone né- cessaire à l’implantation de l’embryon et à son maintien durant les premières semaines.
En absence de fécondation, le corps jaune arrête son fonctionnement après 14 jours ce qui entraîne une chute hormonale en œstrogènes et progestérone et provoque les règles.
Pour permettre l’obtention d’une grossesse, les 3 facteurs suivants jouent un rôle primordial:
- le facteur ovarien, représenté par une production hormonale correcte du follicule, ainsi que par une aptitude normale de l’ovocyte à la fécondation et au développement embryonnaire,
- le facteur mécanique, représenté par des trompes perméables ainsi qu’une cavité utérine normale
- le facteur masculin représenté par un sperme de qualité suffisante.

1. Première consultation
Sur conseil de votre gynécologue, médecin traitant, ou à votre propre initiative, vous prenez rendez-vous pour une consultation auprès d’un des médecins référents en médecine de reproduction. Ainsi il s’agit éventuellement du premier contact avec la médecine de la reproduction, tout comme il est possible que vous ayez déjà suivi des traitements spécifiques.
Lors de cette première consultation, le gynécologue réalise tout d’abord une anamnèse complète qui reprend les antécédents gynéco-obstétricaux, médicaux et chirurgicaux, ainsi que les antécédents familiaux. Les habitudes de vie et l’exposition à des facteurs de risque d’infertilité comme par exemple certaines addictions (tabac, cannabis, alcool…), des anomalies pondérales (obésité ou maigreur), ou encore l’exposition à des risques environnementaux et professionnels sont importants à noter.
L’examen clinique gynécologique n’est pas systématique lors de cette première consultation. Il dépend du moment du dernier examen gynécologique et des points d’appel à l’anamnèse. En effet il est important de s’assurer de la normalité de l’anatomie de l’appareil génital féminin, aussi bien par un examen clinique gynécologique, que par un examen échographique. En échographie il est possible de vérifier le volume et la régularité de l’utérus et de l’endomètre, ainsi que l’aspect et la position des ovaires.
En fin de consultation sont prescrits les examens complémentaires qui sont indispensables à l’identification des causes de l’infertilité et à l’orientation du traitement.
2. Mise au point chez la femme
La détermination de la réserve ovarienne
La détermination de la réserve ovarienne sert à évaluer la fonctionnalité de l’ovaire par un bilan sanguin et une échographie pelvienne en début de cycle au moment des règles (entre le deuxième et le quatrième jour).
L’échographie sert principalement à compter et à mesurer tous les petits follicules en croissance en début du cycle. Elle est réalisée par voie endovaginale, plus précise que la voie abdominale. La vessie n’a donc pas besoin d’être remplie pour cet examen.
La prise de sang consiste en un bilan hormonal (dosage de FSH, LH, œstradiol, hormone anti-mullé- rienne), qui, réalisés en début de cycle (J2-J4), donne des informations sur la capacité de l’ovaire à répondre à un traitement de stimulation.
L’Hystérosalpingographie (HSG)
L’hystérosalpingographie sert à vérifier la régularité de la cavité utérine ainsi que la perméabilité des trompes. Elle évalue donc le facteur mécanique.
Il s’agit d’un examen radiologique, réalisé en position couchée, lors duquel un produit de contraste est injecté par le col de l’utérus. Des clichés radiologiques successifs vont permettre d’observer la migration du produit de contraste qui tout d’abord va remplir la cavité utérine pour ensuite diffuser à travers les trompes jusque dans la cavité abdominale.
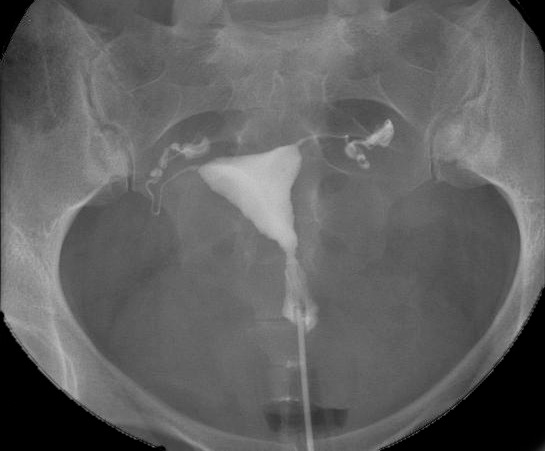
Grâce à cet examen on peut mettre en évidence une anomalie utérine, comme un accolement des parois (synéchie), un fibrome ou encore un polype. Au niveau des trompes, on peut conclure à un éventuel obstacle si le produit de contraste s’accumule en amont et que l’on ne le retrouve pas au niveau de la cavité abdominale en fin d’examen.
Il faut noter que cet examen peut donner lieu à un inconfort qui ressemble à des règles douloureuses. La gêne éventuellement ressentie est due à la distension de la cavité utérine et elle diminue donc rapidement après l’examen.
Il faut dire que l’hystérographie est le seul examen qui permet de vérifier la perméabilité tubaire sans devoir subir une anesthésie générale, comme c’est le cas dans le cadre d’une laparoscopie exploratrice.
Info pratique sur l'HSG : Le 1er jour des règles vous téléphonez dans le service de radiologie du Centre Hospitalier de Luxembourg (CHL) au 4411-6821 afin de fixer un rendez-vous entre le dernier jour des règles et le 12e jour du cycle. Il convient de signaler toute allergie connue, notamment celle à l’iode. Parfois le gynécologue vous prescrit un médicament antispasmodique pour diminuer la contractilité utérine au moment de l’examen ainsi qu’un antibiotique par voie vaginale et/ou orale afin d’éviter une propagation d’une infection vaginale éventuelle.
L'hystérioscopie
Si l’hystérosalpingographie (HSG) permet de visualiser indirectement la cavité endo-utérine et les trompes, l’hystéroscopie (HSC) permet l’inspection directe sous contrôle de la vue de l’intérieur de l’utérus. L’examen est réalisé à l’aide d’une très fine caméra qui est introduite par le vagin à travers le col de l’utérus jusque dans la cavité utérine. Afin de pouvoir examiner correctement cette dernière, la cavité sera distendue conjointement par du liquide (eau physiologique).
Le but de cet examen est de vérifier l’absence d’anomalie de la cavité utérine, y compris au niveau de l’arrivée des trompes. En même temps, l’introduction de la caméra à travers le canal cervical permet d’évaluer la qualité de ce passage dont les relis muqueux dessinent «l'arbre de vie». Le col est en effet délimité par deux orifices: l’un, externe et visible dans le fond du vagin, et l’autre, interne, qui marque le départ de la cavité endo-utérine. Au niveau de l’orifice interne, on peut être confronté à un léger rétrécissement accompagné d’un changement d’angle entre le col et la cavité utérine.
Dans certains cas, il peut être utile de vérifier l’état de la cavité utérine et le passage à travers le col avant un traitement par FIV/ICSI, vu que le ou les embryons obtenus vont être placés dans l’utérus à l’aide d’un fin cathéter.
Parfois, l’examen peut donner lieu à un inconfort qui ressemble à des règles douloureuses, mais il ne né- cessite pas d’anesthésie. La gêne éventuellement ressentie est due à la distension de la cavité utérine et elle diminue donc rapidement après l’examen.
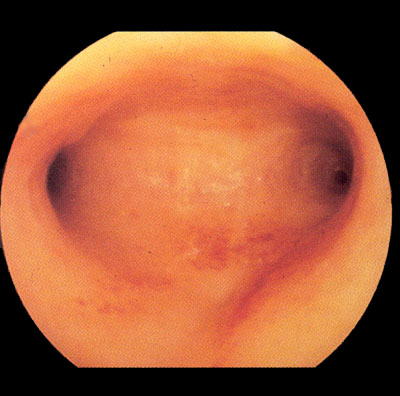
Cavité endo-utérine, Ostium tubaire droit et gauche (Passage vers les trompes)
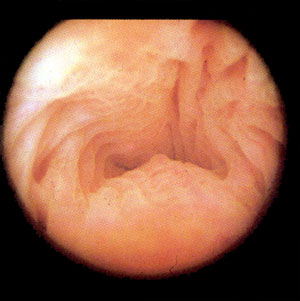
Canal endocervical, «Arbre de vie»
Info pratique pour l'hystérioscopie : Le premier jour des règles vous téléphonez entre 8h00 et 12h00 au 4411-3230 (secrétariat), afin de fixer un rendez-vous pour une HSC ambulatoire qui sera réalisée après les règles. Si le premier jour des règles est un jour de W.-E. ou un jour férié, vous té- léphonez le premier jour ouvrable.
3. Mise au point chez l'homme
Le spermogramme
L’examen des caractéristiques du sperme est au centre du bilan masculin. Il nécessite un recueil au laboratoire, par masturbation, dans un flacon adapté. Il permet de recherche principalement les anomalies suivantes:
- Un nombre insuffisant de spermatozoïdes, appelé OLIGOSPERMIE (<15 M/ml ou <39 M/éjaculat) ou AZOOSPERMIE, si aucun spermatozoïde n’est retrouvé dans le sperme.
- Une mobilité insuffisante des spermatozoïdes, appelée ASTHENOSPERMIE (<32% mobilité progressive ou <40% mobilité totale).
- Une proportion trop importante de spermatozoïdes morts, appelée NECROSPERMIE (<58% de formes vivantes).
- Une proportion trop importante de spermatozoïdes présentant des anomalies de forme, appelée TERATOSPERMIE (<4% de formes normales).
Diverses combinaisons de ces anomalies sont fréquemment observées.
Est rajouté à cet examen le plus souvent une spermoculture pour exclure une infection éventuelle des voies génitales masculines.
Dans certains cas, un test de fragmentation de l’ADN des spermatozoïdes peut être proposé chez des couples qui ne parviennent pas à obtenir de grossesse évolutive, soit en raison d’échecs d’implantation successifs, soit dans le cadre de fausses couches à répétition. En effet, dans ces situations, une proportion anormalement élevée de spermatozoïdes présentant un ADN fragmenté est parfois mise en évidence.
Info pratique pour l'homme : Vous prenez un RDV pour un spermogramme en appelant le secrétariat du laboratoire de PMA (4411- 6520) entre 8.00 et 12.00H. Lors de la prise de rendez-vous, la secrétaire vous demandera de lire le libellé exact de votre ordonnance, de manière à savoir quels examens sont demandés précisément. Le jour du RDV vous êtes prié de vous munir de votre carte d’identité, de votre carte d’assuré social et de votre ordonnance. Le prélèvement est réalisé au laboratoire, dans une pièce aménagée pour cela. Il vous sera également demandé de respecter une abstinence sexuelle de deux à sept jours avant l’examen.
Le test post-coïtal (test de Hühner)
Ce test consiste à évaluer la glaire cervicale 9 à 14 heures après un rapport sexuel, en déterminant les caractéristiques physiques de la glaire (abondance, aspect, filance, cristallisation), ainsi que la présence et la mobilité des spermatozoïdes dans la glaire.
Ce test évalue ainsi à la fois le versant masculin (qualité du sperme) et féminin (qualité de la glaire) de l’infertilité. Toutefois, en raison de sa valeur diagnostique limitée, ce test n’est plus réalisé systématiquement.
Info pratique pour la femme : Dès le premier jour du cycle, vous téléphonez au secrétariat du laboratoire de PMA (4411-6520) entre 8.00 et 12.00H, afin de fixer un rendez-vous pour un test post-coïtal qui va être réalisé au moment le plus proche de l’ovulation. Il consiste en un examen gynécologique lors duquel la glaire cervicale est aspirée au niveau du col pour être analysée par la suite au microscope
4. Consultations complémentaires
4.1 Consultation sage-femme
La sage-femme coordinatrice vous accompagne tout au long de votre prise en charge dans notre service.
Elle a plusieurs rôles:
- elle coordonne les différents soins, consultations, actes techniques et examens complémentaires nécessaires à votre prise en charge,
- elle réalise une partie des échographies et des prises de sang, • elle coordonne les résultats journaliers de votre traitement et vous transmet les consignes du mé- decin pour la suite de la stimulation,
- elle assiste le médecin pour certains actes techniques,
- elle vous reçoit en consultation spécialisée (sur RDV au tél: 4411-6520) afin de passer en revue le traitement et de répondre aux questions avant de débuter le traitement ou pendant le traitement,
- elle vous guide pendant votre traitement si vous avez des doutes ou des questions.
La sage-femme assure une écoute quotidienne et reste à votre entière disposition en cas de questions, doutes ou problèmes inhérents à votre suivi d’infertilité.
4.2 Consultation en biologie de la reproduction
Une consultation avec le médecin biologiste responsable du laboratoire de PMA peut-être proposée au couple. Cette consultation est particulièrement utile avant une première tentative de FIV, avant le recours à une procréation avec tiers donneur de gamètes ou devant tout questionnement par rapport aux aspects biologiques de la prise en charge en PMA.
Au cours de cette consultation, le biologiste:
- expliquera le déroulement pratique, les chances de grossesse, les aspects biologiques, la congélation embryonnaire, les techniques particulières et les problèmes techniques pouvant se présenter au cours de la prise en charge,
- fera le point avec le couple, en cas d’absence de grossesse après plusieurs tentatives de FIV/ICSI, et donnera des précisions sur la qualité des embryons et leur développement et les possibilités d’amélioration,
- expliquera les particularités du recours à une procréation avec tiers donneur de gamètes,
- complétera si besoin l’anamnèse des deux membres du couple dans le dossier médical.
4.3 Consultation d'andrologie
Lorsque l’examen du sperme a donné lieu à des résultats anormaux, ou lorsqu’il existe un signe clinique ou un antécédent évocateur, le bilan sera complété sur le plan masculin au cours d’une consultation d’andrologie.
Cette consultation est réalisée généralement par un urologue et comporte une anamnèse complète (antécédents, traitements en cours, exposition à des substances toxiques…), ainsi qu’un examen clinique à la recherche d’éventuelles anomalies de l’appareil génital, telles que le varicocèle (une varice à l’intérieur des bourses).
Selon les cas, des examens complémentaires pourront éventuellement être demandés:
- Prise de sang pour des dosages hormonaux.
- Échographie des testicules et/ou de la prostate.
- Analyses complémentaires du sperme: spermoculture (recherche de bactéries), test de migration (préparation de sperme en vue d’une PMA), test de fragmentation de l’ADN (témoin de l’intégrité du noyau des spermatozoïdes)… etc.
- Bilan génétique (en cas d’altération sévère du sperme): caryotype (analyse des chromosomes), recherche de microdélétions du chromosome Y (perte de certaines régions qui contrôlent la formation des spermatozoïdes), recherche de mutations du gène CFTR (gène de la mucoviscidose)… etc.
4.4 Consultation de soutien psychologique
Le rôle de l’entretien psychologique consiste à informer, conseiller, soutenir, guider les personnes au cours des différentes phases de la prise en charge, à surmonter la blessure psychologique, le «mal-être», la déstabilisation du couple, le questionnement sur soi, aider à assimiler le traitement, gérer le risque de l’échec, et trouver des perspectives alternatives en cas de besoin.
4.5 Consultation en hypnose
Le processus de Procréation Médicalement Assistée est souvent perçu comme stressant et angoissant. Les techniques de relaxation par hypnose vous permettront de vous préparer de façon optimale aux différentes phases du traitement.
L’hypnose (ou détente profonde) permet ainsi de:
- mieux gérer ses peurs et d’adopter une attitude positive,
- apprendre à utiliser ses propres ressources,
- mettre en harmonie le corps et l’esprit et d’augmenter le bien-être physique et mental. Les séances s’adaptent entièrement à vos besoins et offrent des moments de bien-être, de détente et de relâchement.
Pour tout renseignement, n'hésitez pas à nous contacter: info@hypnobalance.lu
4.6 Consultation en sexologie
Au niveau des relations intimes, il est difficile de présumer des difficultés rencontrées chez chaque personne. En effet, le rapport entre sexualité et fertilité est complexe et se traduit différemment selon le couple.
Au cours d’un traitement de procréation médicalement assistée, les relations sexuelles peuvent devenir plus techniques. De fait, la sexualité peut être perturbée chez certains couples durant cette période, les buts et les moments des rapports étant modifiés, calculés. La médicalisation de l’infertilité pourrait, dans ce cadre, déstabiliser l’harmonie sexuelle du couple, l’enjouement et la fréquence des rapports sexuels.
4.7 Consultation de tabacologie
De nombreuses études ont démontré l’impact négatif de la fumée de tabac aussi bien sur la fertilité naturelle que sur les chances de succès en PMA. Ainsi, chez la femme, le tabac allonge le délai de conception, augmente le risque de fausse-couche et porte atteinte à la réserve ovarienne; chez l’homme, il altère les paramètres spermiologiques et la qualité du matériel génétique véhiculé par le spermatozoïde. Le tabagisme parental peut également avoir des consé- quences sur la santé des enfants.
Choisir et décider d’arrêter de fumer augmente vos chances d’avoir un enfant, en améliorant la qualité de l’ovulation, des ovocytes et de l’implantation embryonnaire, de même que la qualité du sperme (ainsi que d’éventuels problèmes d’érection).
4.8 Autres
- Consultation d'endocrinologie
- Consultation de diététique
5. Facteurs de risque de l'infertilité
Ces facteurs ne sont pas des causes d’infertilité à proprement parler, mais leur présence augmente la probabilité que la fertilité du couple soit altérée.
5.1 Âge de la femme
• Principal facteur de pronostic en termes de chances de grossesse évolutive, en fertilité naturelle comme en PMA.
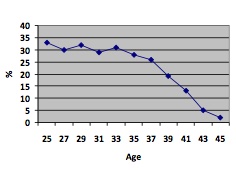
Effet de l'âge de la femme sur le taux de succès en FIV
5.2 Activité sexuelle
La fréquence des rapports sexuels et leur chronologie par rapport à la période fertile du cycle menstruel sont importantes à prendre en considération et seront abordés en consultation clinique.
5.3 Exposition à des toxiques
- Produits de consommation: Tabac, alcool, cannabis et autres drogues allongent le délai de conception et réduisent fortement les chances de succès en PMA. Il est important que le médecin soit informé objectivement de ce type de consommation de manière à pouvoir proposer une prise en charge complémentaire en vue d’un sevrage.
- Toxiques professionnels: souvent négligées, les substances reprotoxiques auxquelles sont soumis les patients de façon régulière doivent être recherchées, éventuellement avec l’aide du médecin du travail du patient. Des facteurs physiques tels que la chaleur, dont l’effet sur la spermatogenèse est bien connu, peuvent également être en cause.
- Certains médicaments peuvent avoir un impact délétère sur la fertilité; il est donc également important que le patient signale tous les produits pharmaceutiques utilisés, que ce soit sur prescription médicale ou en automédication.
5.4 Autres facteurs
- Anomalies pondérales: surpoids et obésité sont associés avec de moindres chances de grossesse en PMA, que ce soit chez la femme ou chez l’homme. À l’inverse, un poids insuffisant (dénutrition, anorexie…) peut-être responsable d’une dérégulation des fonctions ovariennes.
- Certaines pathologies générales retentissent sur la fertilité et les chances de succès en PMA. Toute information sur votre état de santé peut donc avoir une importance dans la prise en charge pour infertilité.
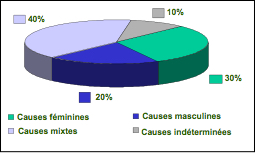
Causes d'infertilité
6. Causes masculines
Les causes masculines peuvent être divisées schématiquement en troubles de l'éjaculation et en troubles de la qualité du sperme.
6.1 Troubles de l'éjaculation
Ils répondent à différents mécanismes:
- Anatomiques: malformations du pénis…
- Neurovasulaires: diabète, traumatismes de la moelle épinière…
- Psychogènes
Un cas particulier est représenté par l’éjaculation rétrograde, au cours de laquelle le sperme, au lieu d’être émis par l’urètre, remonte dans la vessie. Cette anomalie peut être due au diabète, à la chirurgie pelvienne, aux traumatismes médullaires… Dans ce cas, des spermatozoïdes utilisables en PMA peuvent être récupérés dans les urines après masturbation. Il sera alors demandé au patient de boire de l’eau de Vichy la veille de l’examen et le matin même pour rendre les urines plus alcalines (l’acidité naturelle des urines étant délétère pour les spermatozoïdes).
6.2 Troubles de la qualité du sperme
Ces anomalies documentées par les résultats du spermogramme (oligospermie, asthénospermie, né- crospermie, tératospermie) répondent à de nombreux mécanismes possibles:
- Génétiques: anomalies chromosomiques (ex. syndrome de Klinefelter), microdélétions du chromosome Y…
- Dystrophiques: maldescente testiculaire (cryptorchidie ou ectopie testiculaire).
- Infectieux: prostatites, épididymites, aiguës ou chroniques, éventuellement à l’origine d’obstructions de la voie séminale.
- Stase veineuse: présence de varices sur les veines testiculaires (= varicocèle).
- Malformatifs: agénésie d’une partie de la voie séminale (canal déférent, vésicules séminales…). Lorsque ces anomalies sont bilatérales, il convient de rechercher la présence de mutations dans le gène de la mucoviscidose, de manière à préciser les risques éventuels pour la descendance.
- Idiopathiques: c’est ainsi que sont qualifiées les situations, fort nombreuses, où aucune cause ne peut être retrouvée.
Afin d’optimiser ce bilan étiologique chez l’homme, une consultation spécialisée auprès d’un urologue/ andrologue sera proposée. Cette consultation peut éalement aboutir à des traitements à mettre en œuvre avant le recours à la PMA.
Dans certains cas d’azoospermie, il peut être nécessaire de réaliser une biopsie testiculaire afin de rechercher des spermatozoïdes utilisables en PMA. Cette biopsie sera réalisée préalablement à la PMA, les fragments biopsiés seront examinés au laboratoire de PMA et les éventuels spermatozoïdes retrouvés seront congelés.
6.3 Altération prévisible de la fertilité masculine
Dans certains cas, il est possible d’anticiper une dégradation des paramètres spermiologiques. C’est notamment le cas lorsque le patient doit subir un traitement potentiellement stérilisant, tel qu’une chimiothérapie ou une radiothérapie pelvienne. Dans ces cas il convient de réaliser une autoconservation (congélation) de sperme préalablement. Celleci peut également être proposée lorsqu’il existe des problèmes de recueil, un spermogramme très variable dans le temps, une altération très marquée du spermogramme au cours des tentatives successives de PMA ou encore avant une vasectomie (stérilisation volontaire par section des canaux déférents).
7. Causes féminines
7.1 La stérilité tubaire
L’obstruction tubaire, lorsqu’elle est bilatérale, entraine une stérilité définitive. Elle peut être due à une infection pelvienne, éventuellement passée inaperçue, à une chirurgie abdominopelvienne à l’origine d’adhérences ou à l’endométriose (voir plus loin). L’obstruction tubaire est dépistée à l’hystérosalpingographie, mais nécessite le plus souvent un complément d’investigation par une laparoscopie au cours de laquelle un geste réparateur peut également être tenté dans certains cas.
7.2 Les troubles de l'ovulation
Très fréquemment en cause dans l’infertilité, un trouble de l’ovulation peut être suspecté devant:
- Des troubles menstruels tels qu’une spaniomé- norrhée (cycles très longs) ou une aménorrhée (absence de cycles spontanés).
- Une pilosité anormale.
- Un développement anormal des caractères sexuels secondaires.
- Des images évocatrices à l’échographie des ovaires.
- Des résultats anormaux pour les dosages hormonaux réalisés en tout début de cycles (J2-J4): FSH, LH, E2, AMH, PRL, TSH.
Parmi les causes les plus fréquentes à l’origine des troubles de l’ovulation, on peut citer le syndrome des ovaires micropolykystiques (SOMPK) et les hyperprolactinismes (sécrétion anormale de prolactine, l’hormone de la lactation).
7.3 Endométriose
Définie par la présence d’implants de muqueuse uté- rine en dehors de l’utérus, cette maladie peut être asymptomatique ou au contraire se traduire par des douleurs pelviennes, surtout au moment des règles (dysménorrhée) et lors des rapports sexuels (dyspareunie). Elle peut entrainer une infertilité soit par effet mécanique (obstruction tubaire p. ex.), par effet toxique pour l’embryon (sécrétion de facteurs inflammatoires), ou par altération de la réserve ovarienne (séquellaire d’interventions chirurgicales portant sur les ovaires.
7.4 Anomalies utérines
Plus fréquemment en cause dans les fausses couches que dans l’infertilité proprement dite, ces anomalies comprennent les malformations utérines, les fibromes (tumeurs bénignes du muscle utérin) et les polypes endocavitaires (tumeurs bénignes de la muqueuse utérine).
Dépistées à l’hystérosalpingographie ou à l’échographie pelvienne, ces anomalies nécessitent le plus souvent un complément d’investigation par une hystéroscopie au cours de laquelle un geste réparateur peut également être réalisé dans certains cas.
7.5 Autres causes
D’autres causes peuvent contribuer au problème d’infertilité, tels qu’une sécrétion insuffisante de glaire cervicale par les glandes du col de l’utérus, ce qui empêche l’ascension des spermatozoïdes dans les voies génitales féminines. Ces cas peuvent être liés à des troubles de l’ovulation ou à un antécédent de conisation large.
7.6 Altération prévisible de la fertilité féminine
Dans certains cas, il est possible d’anticiper une dé- gradation de la réserve ovarienne. C’est notamment le cas lorsque la patiente doit subir un traitement potentiellement stérilisant, tel qu’une chimiothérapie ou une radiothérapie pelvienne.
Dans ces cas, il convient de décider avec l’équipe de PMA, quelle mesure de préservation de la fertilité sera la mieux adaptée (congélation d’ovocytes, d’embryons, de tissu ovarien…).
1. Induction d'ovulation simple
Si le bilan étiologique a montré uniquement un trouble de l’ovulation, en absence d’autres causes chez un couple jeune, il convient de tenter dans un premier temps de corriger ce problème par une stimulation ovarienne.
Ce traitement a pour but d’obtenir un ou deux follicules mûrs et comporte:
- soit une prise médicamenteuse par voie orale de clomifène (CLOMID®) pendant 5 jours par cycle, surtout chez les patientes qui ont des cycles irréguliers voire absents,
- soit des injections quotidiennes de FSH par voie sous-cutanée à partir du 3e, 4e ou 5e jour du cycle (FSH recombinante: GONAL-F®, PUREGON® ou FSH d’extraction: MENOPUR®, FOSTIMON®) Le traitement prend en moyenne 13 jours à partir du premier jour des règles.
Ces traitements nécessitent impérativement une surveillance (monitorage) de la réaction des ovaires à la stimulation, par échographies et prises de sang (environ 3 contrôles par cycle), ceci afin de:
- vérifier l’existence d’une croissance folliculaire,
- vérifier que celle-ci n’est pas excessive, exposant ainsi la patiente à un risque de grossesse multiple.
Les informations obtenues grâce à ce monitorage permettent de cibler les rapports sexuels vers le moment de l’ovulation. En effet, une fois la taille folliculaire optimale atteinte, l’ovulation peut se produire de façon spontanée (si un pic de LH est détecté à la prise de sang) ou bien elle peut être déclenchée par une injection intramusculaire d’hCG (PREGNYL®).
Pour les modalités pratiques concernant ce monitorage, veuillez vous reporter au chapitre suivant «Traitements de stimulation: en pratique».
2. Insémination artificelle intra-utérine (IIU)
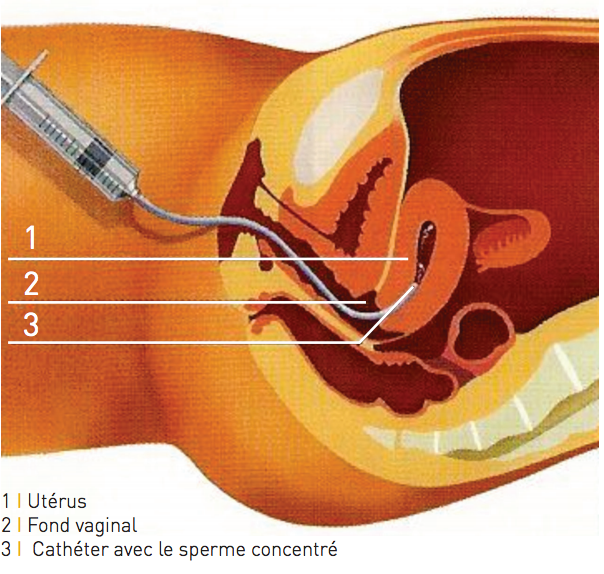
Il s’agit d’une technique simple et indolore, dont le but est d’amener plus de spermatozoïdes plus loin dans les voies génitales féminines (et donc plus près du site de fécondation). Concrètement, le sperme frais ou congelé du partenaire (IAC) voire le sperme congelé d’un donneur (IAD) est préalablement préparé au laboratoire, puis injecté, à l’aide d’un petit cathéter, dans la cavité utérine au moment de l’ovulation.
Indications:
- Certaines anomalies du col de l’utérus ou de la glaire cervicale.
- Les infertilités idiopathiques (infertilité d’origine inconnue).
- Anomalies modérées des paramètres spermatiques
- Troubles de l’éjaculation
- Recours à un sperme de donneur
Conditions :
- Chez la femme: au moins une trompe perméable.
- Chez l’homme: au minimum 1 million de spermatozoïdes mobiles progressifs après préparation du sperme.
La préparation de sperme
La préparation du sperme au laboratoire a pour but de séparer les spermatozoïdes du liquide séminal, de sélectionner les spermatozoïdes les plus mobiles et de concentrer la préparation en un faible volume, adapté à la technique utilisée.
L'insémination intra-utérine en pratique
L’insémination est réalisée le plus souvent le lendemain du pic LH ou le surlendemain du déclenchement par le PREGNYL: vous serez donc prévenue du jour de l’insémination 1 ou 2 jours auparavant. Il vous sera demandé vous munir d’une pièce d’identité et de venir avec la vessie remplie (ce qui permet de redresser l’utérus dans l’axe du corps et de faciliter l’insémination).
Afin d’optimiser l’organisation de l’activité du service, chaque médecin a un jour fixe dans la semaine pour faire les inséminations.
L’insémination est réalisée en position gynécologique après pose d’un spéculum et exposition du col de l’utérus. La préparation de sperme est montée dans le cathéter, puis ce dernier est introduit dans la cavité utérine, en passant par le col (Figure 12). Il s’agit d’une technique tout à fait indolore. Après l’insémination, vous vous reposerez quelques minutes en position allongée.
Parfois, lorsque le passage du col s’avère moins aisé, l’insémination peut être réalisée sous échoguidage abdominal.
Info pratique pour les femmes : La croissance folliculaire nécessite le plus souvent une induction d’ovulation comme pour l’IS (cf ci-dessus), par clomifène (voie orale) ou FSH (voie sous-cutanée), afin d’optimaliser la croissance mono- ou bifolliculaire.
Dans certains cas, le médecin proposera de réaliser l’IIU en cycle spontané, sans traitement de stimulation ovarienne.
Qu’il y ait stimulation ovarienne ou non, un monitorage par échographies et dosages hormonaux sera réalisé, pour surveiller la croissance du ou des follicules (maximum 2) et faire coïncider l’insémination avec le moment de l’ovulation. Celle-ci peut, là encore, se produire de façon spontanée (si un pic de LH est détecté à la prise de sang) ou être déclenchée par une injection de PREGNYL®.
Pour les modalités pratiques concernant ce monitorage, veuillez vous reporter au chapitre suivant «Traitements de stimulation: en pratique».
Info pratique pour les hommes : Le jour de l’insémination, en cas d’insémination avec le sperme éjaculé, vous êtes convoqué environ deux heures avant l’insémination. Une pièce d’identité vous sera demandée. Le sperme devra être recueilli impérativement au laboratoire. Vous y serez installé dans une pièce dédiée à cette activité.
Après l'insémination
Aucune précaution particulière n’est nécessaire après l’insémination.
Dans certains cas, afin d’optimiser la phase lutéale qui est la 2e phase du cycle, votre médecin vous prescrira le jour de l’insémination des comprimés de progestérone naturelle, UTROGESTAN®, par voie vaginale.
Une prise de sang sera réalisée 14 jours après l’insé- mination afin de savoir si vous êtes enceinte. Les taux de grossesse par cycle en IIU sont de 10-12% en IAC et de 15-18% en IAD.
Remarque: Il est évident que vous pouvez avoir des rapports sexuels les jours avant et après l’insémination. Il est même conseillé d’avoir des rapports sexuels 2 jours avant l’insémination. (sauf la veille de l’insémination).
Insémination artificielle avec sperme de donneur (IAD)
Le recours à un sperme de donneur peut être indiqué en cas de:
stérilité masculine définitive (azoospermie avec tentative infructueuse ou impossibilité d’extraire des spermatozoïdes à partir d’une biopsie testiculaire),
infertilité masculine et renoncement à une PMA intraconjugale jugée trop lourde (FIV ICSI après biopsie testiculaire),
risque de transmission à l’enfant d’une maladie grave et incurable.
Il s’agit d’une démarche qui doit être mûrement réfléchie quant à ses modalités de mise en œuvre et à ses conséquences (filiation, secret face à l’enfant, anonymat du donneur…). Dans ce contexte, une consultation auprès d’un psychologue et/ou psychiatre adjoint à l’équipe de PMA est indispensable.
Le laboratoire de PMA ne disposant pas d’une autorisation ministérielle pour faire offre de gamètes directement, le recours à une banque de sperme internationale vous sera proposé. Ainsi, il sera le plus souvent possible d’apparier le donneur et le futur père selon des caractéristiques phénotypiques (ethnicité, morphotype, groupe sanguin…). Une fois le choix validé par le laboratoire de PMA, la commande sera effectuée par l’intermédiaire du laboratoire. Le coût des paillettes de donneur et les frais de transport seront à la charge du couple demandeur.
En bref :
- Stimulation ovarienne mono- ou bifolliculaire par anti-oestrogènes (per os) ou des Gonadotrophines (inj. sous-cutanées)
- Déclenchement de l’ovulation
- Préparation du sperme
- Insémination intra-utérine
3. Fécondation In Vitro
Au cours d’une fécondation in vitro (FIV) la rencontre de l’ovocyte et du spermatozoïde se fait au laboratoire, en dehors du corps de la femme. Il faut ainsi disposer au laboratoire à la fois des spermatozoïdes et des ovocytes. Ceci implique pour Monsieur un recueil de sperme, comme pour une insémination. En revanche, pour Madame, la technique est bien plus complexe qu’une insémination intra-utérine, car non seulement, la stimulation ovarienne est nettement plus intense, mais, une fois les follicules mûrs, les ovocytes doivent être retirés des ovaires au cours d’une geste chirurgical: la ponction folliculaire.
Cette ponction est réalisée au bloc opératoire de la Maternité, le plus souvent sous anesthésie générale, par voie transvaginale. Elle consiste à introduire, sous contrôle échographique, une aiguille dans les follicules ovariens pour en aspirer le contenu, le liquide folliculaire. Afin d’optimiser l’organisation de l’activité du service, chaque médecin a un jour fixe dans la semaine pour faire les inséminations. Les liquides ponctionnés sont ensuite acheminés au laboratoire, pour être examinés sous une loupe, ce qui permet d’identifier les ovocytes. Pour organiser la fécondation au laboratoire, deux techniques sont disponibles:
FIV Classique
Dans cette technique qui existe depuis 1978, les ovocytes sont mis en présence d’un grand nombre de spermatozoïdes préalablement préparés, placés dans une boîte de culture et incubés dans une étuve. Ainsi, la pénétration du spermatozoïde dans l’ovule et la fécondation se font de manière spontanée, à condition que le sperme soit normal ou modérément altéré.
Indications:
- Stérilité mécanique: lorsque les trompes sont obstruées / imperméables et qu’elles ne peuvent être réparées chirurgicalement.
- Endométriose.
- Stérilité masculine: en cas de diminution modérée de la qualité des spermatozoïdes.
- Échec des inséminations intra-utérines.
- Stérilité inexpliquée (idiopathique)
FIV ICSI (Intracytoplasmic sperm injection)
Si le sperme est de qualité insuffisante pour que les spermatozoïdes puissent pénétrer spontanément dans l’ovocyte, la technique de FIV ICSI, plus récente (première naissance en 1992), permet d’introduire directement le spermatozoïde à l’intérieur de l’ovocyte. L’indication principale de cette technique est donc l’infertilité masculine sévère, dans laquelle les paramètres du sperme sont très altérés. Ainsi, l’ICSI est réalisée avec du sperme frais ou congelé, de même qu’après prélèvement chirurgical de spermatozoïdes (par ponction épididymaire ou par biopsie testiculaire).
Dans certaines autres situations, le recours à l’ICSI peut être discuté, malgré des paramètres spermiologiques théoriquement compatibles avec une FIV classique; c’est le cas par exemple en cas d’infertilité ancienne avec échec de nombreux traitements antérieurs.
En cas de doute, il est possible de réaliser une FIV mixte, dans laquelle la moitié des ovocytes recueillis sont inséminés selon la technique classique tandis que les autres sont préparés en vue d’une technique d’ICSI.
Transfert In Utero
Après une fécondation réussie, et une culture au laboratoire pendant 2 ou 3, voire parfois 5 jours, un ou deux embryons sont replacés dans la cavité utérine.
Info pratique : Pour stimuler les ovaires en FIV/ICSI, il existe plusieurs types de schémas différents. Une fois la mise au point terminée, votre gynécologue, ayant à sa disposition tous les renseignements nécessaires, choisira le protocole de stimulation le plus adapté à votre cas.
Les détails du traitement et des modalités de surveillance (monitorage) vous sont présentés dans le chapitre «Votre prise en charge en pratique». Ils vous seront également expliqués au cours de la consultation avec la sage-femme de PMA.
Les détails de ce qui se passe au laboratoire vous sont présentés dans le chapitre «Le travail au laboratoire». Ce travail donne lieu à un certain nombre d’options et de choix techniques dont vous pourrez discuter au cours de la consultation avec le biologiste.
1. Formalités administratives
Prise en charge financière
La prise en charge financière de la FIV par la Caisse Nationale de Santé (CNS) n’est assurée que suite à l’accord préalable dont la demande sera faite par le gynécologue du service de PMA avant le début du traitement.
Les frais de laboratoire et des examens médicaux sont totalement pris en charge par la caisse, ceux des médicaments à 80%, pour autant que la patiente remplisse les critères établis suivants:
- La ponction a lieu avant l’âge de 43 ans accomplis.
- Le quota maximal de 4 tentatives prises en charge par la CNS n’est pas encore atteint. Actuellement, la tentative est définie par la CNS comme une ponction folliculaire suivie d’une culture embryonnaire.
- Quant à l’âge de l’homme, il n’est pas pris en compte dans le cadre de la prise en charge par la CNS. Toutefois, pour des raisons éthiques et médicales (augmentation des risques pour la descendance…), notre équipe a fixé à 65 ans l’âge maximal de l’homme au moment de la tentative de PMA. Au-delà de cette limite, une évaluation pluridisciplinaire au cas par cas est requise.
Papiers de consentement éclairé
Toutes les techniques proposées nécessitent votre accord écrit moyennant des formulaires de consentement que votre gynécologue vous remettra en même temps que les explications correspondantes. Ces consentements doivent être renouvelés à chaque tentative.
À titre d’exemple:
- Pour une FIV, vous devez signer les deux papiers de consentement éclairé concernant le traitement en lui-même (FIV classique ou ICSI, voire les deux, avec sperme de conjoint ou de donneur), ainsi que l’éventuelle congélation d’embryons surnumé- raires.
- Pour une IIU, un formulaire de consentement devra également être signé (IAC ou IAD).
2. Le bilan sérologique et la consultation en anesthésie
Bilan sérologique
Pour toute première tentative de PMA ou de congé- lation de gamètes ou d’embryons, il faut que votre dernier bilan sérologique (bilan des maladies virales) (masculin et féminin) ne date pas de plus de 3 mois.
Ces sérologies obligatoires comprennent:
- HIV
- HCV
- HBV: Ag HBs et Ac anti HBc totaux/IgG
- Syphilis
Par la suite, ces sérologies obligatoires devront être recontrôlées, de manière à disposer, à chaque tentative, de résultats datant de moins d’un an. A celles-ci sont ajoutées en fonction du contexte clinique: rubéole, toxoplasmose, CMV, Chlamydiae trachomatis…
Il faut savoir que pour des raisons de sécurité et d’infrastructure, nous ne pouvons actuellement pas accepter dans notre centre des patient(e)s à risque viral, porteurs de certaines sérologies positives, notamment celles pour le HIV, l’HCV (sauf si la charge virale est négative) et l’Ag HBs. En cas de positivité pour un de ces marqueurs, nous vous adressons pour la ponction et le transfert embryonnaire dans un centre spécialisé à l’étranger. La stimulation et le contrôle médical par contre, peuvent être faits au Luxembourg.
La consultation en anesthésie
Si vous suivez un traitement par FIV ou FIV/ICSI une première étape importante est représentée par le prélèvement ovocytaire. Cette ponction est réalisée au bloc opératoire, sous anesthésie générale, locale assistée ou sous anesthésie locale paracervicale simple.
Une consultation chez l’anesthésiste est donc indispensable et sera réalisée en début de traitement de stimulation (une consultation reste habituellement valable pendant 1 an). Vous pourrez prendre un rendez-vous par l’intermédiaire du secrétariat du service de PMA.
3. Les médicaments
En fonction de votre protocole, votre gynécologue vous prescrira les médicaments nécessaires.
Voici un petit résumé du mode d’action des différentes familles de médicaments et d’hormones:
Stimulation folliculaire
- Citrate de Clomifène: CLOMID®
Comprimés par voie orale Anti-oestrogène, stimule indirectement la croissance folliculaire en augmentant la sécrétion de FSH endogène par l’hypophyse.
- Gonadotrophines
FSH recombinante: PUREGON®, GONAL-F® FSH purifiée/LH: MENOPUR® FSH hautement purifiée: FOSTIMON®
Injections sous-cutanées à l’aide d’un stylo ou d’une seringue.
Stimulent les ovaires de manière directe en favorisant la croissance des follicules. Le nombre de ces derniers varie selon la dose et la réceptivité ovarienne.
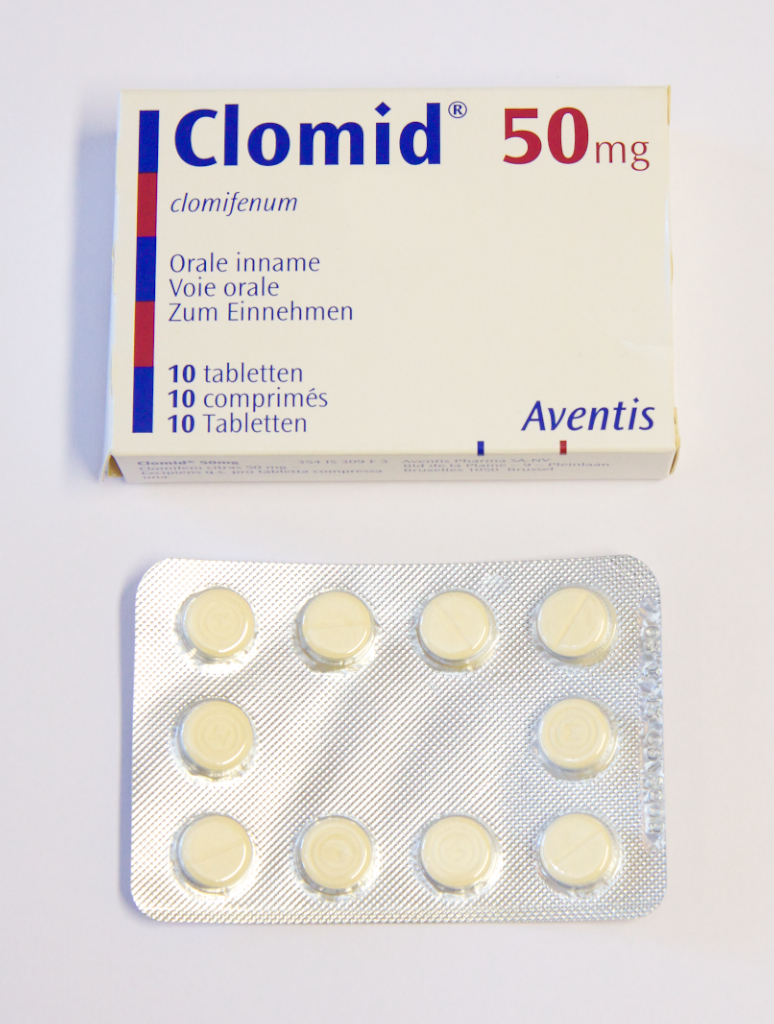

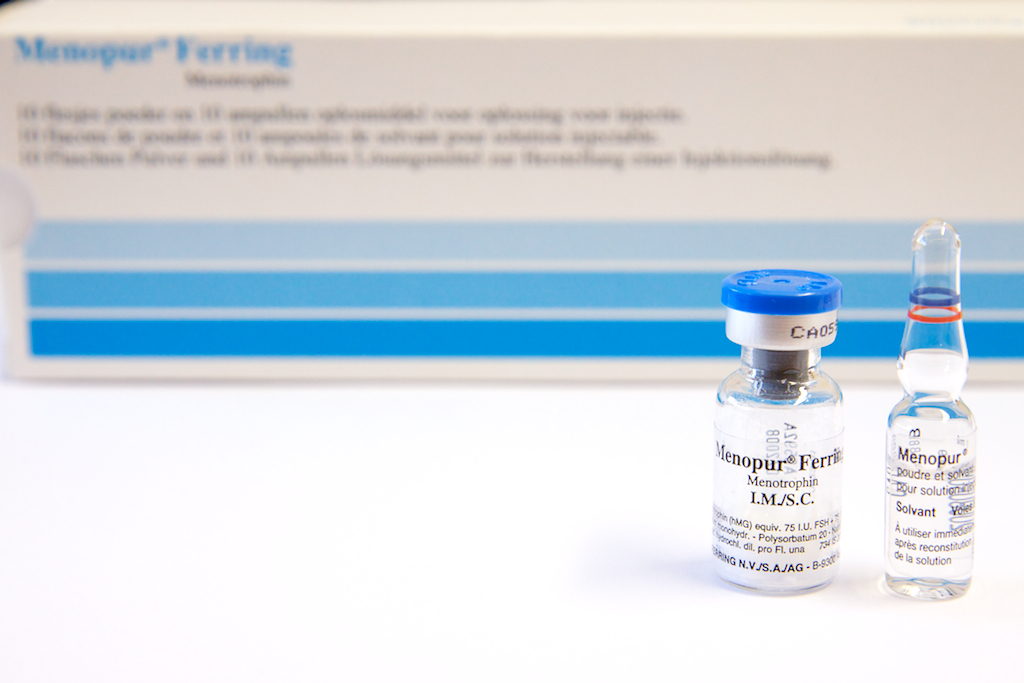
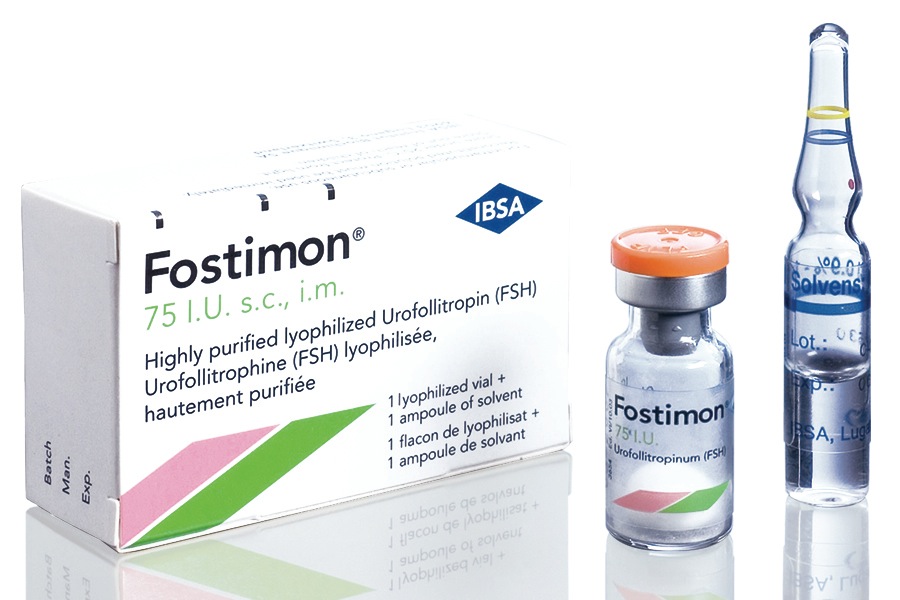
De gauche à droite : Citrate de clomifène (CLOMID), stylo auto-injecteurs (PURGEON et GONAL-F, Poudre et solvant (MENOPUR), poudre et solvant (FOSTIMON)
Blocage hypophisaire
Le but du blocage hypophysaire est d’éviter un pic de LH spontané et donc une ovulation non contrôlée.
• Agonistes du GnRH: (bloqueurs indirects)
- DECAPEPTYL® 3,75 (injection intramusculaire IM unique)
- DECAPEPTYL® 0,1 (injections sous-cutanées SC journalières)
- SUPREFACT® spray nasal 3x/j
Ces médicaments provoquent une stimulation initiale très importante mais de courte durée de l’hypophyse. Ensuite cette dernière se mettra au repos (uniquement pour la sécrétion de FSH et de LH) avec un arrêt transitoire du cycle. Le mécanisme d’action de cette classe de médicaments explique que leur administration précède celle des gonadotrophines.
• Antagonistes du GnRH: (bloqueurs directs)
- ORGALUTRAN®
- CETROTIDE®
Injections sous-cutanées journalières, seringues pré- remplies. Les antagonistes du GnRH bloquent l’hypophyse de fa- çon directe et immédiate, sans hyperstimulation initiale comme dans le cas des agonistes, décrits ci-dessus. Ainsi leur administration se fait en cours de stimulation.
Déclenchement de l'ovulation
• PREGNYL® 5000 UI
Injection intramusculaire à faire par une infirmière à domicile. Provoque l’ovulation 36-40 heures plus tard, ce qui permet de programmer la ponction folliculaire ou l’insémination 2 jours plus tard.
Soutien de la phase lutéale
• Progestérone naturelle: UTROGESTAN® (comprimés - voie vaginale)
Autres
• Pilule contraceptive
Elle bloque l’ovulation et met donc l’ovaire au repos. Ceci permet de synchroniser la cohorte folliculaire en début de cycle et de programmer le début de la stimulation afin de le prévoir en milieu de semaine.
• Progestatifs et/ou Oestrogènes naturels pour programmer les règles
Acide folique
L’acide folique est une vitamine du groupe B (B9) qui permet de réduire significativement le risque de certaines malformations du bébé, en particulier celles de la colonne vertébrale (spina bifida et autres anomalies de fermeture du tube neural).
Ainsi il est recommandé à toutes les femmes ayant un désir de grossesse de prendre un supplément d’acide folique, dès avant la grossesse et pendant les deux premiers mois de la grossesse. La dose recommandée est de 0,4 mg/jour (5 mg/jour en cas d’antécédent de spina bifida).
De gauche à droite : Poudre et solvant (DECAPEPTYL), Poudre et solvant (PREGNYL), Progesterone naturelle (UTROGESTAN)
4. Les injections et le monitorage
Suivant le type de traitement prescrit, la stimulation pourra commencer le premier jour des règles ou plus tard.
Il est important de prévenir le secrétariat le premier jour des règles (tél: 4411-6520 entre 7h00 et 12h00 - téléphonez le premier jour ouvrable).
On vous fixera ainsi le rendez-vous pour la première échographie et prise de sang de contrôle. Si le suivi de la stimulation est assuré par votre gynécologue référent, on vous indiquera le jour de ces examens et c’est vous qui allez le contacter pour fixer ce RDV.
Jusqu’au premier RDV vous allez faire les injections comme indiquées selon votre protocole.
Les injections
Votre médecin vous a remis votre protocole de stimulation où sont précisés les jours et les médicaments à injecter.
La plupart des injections se font dans le tissu souscutané (sous la peau du ventre) en début de soirée. La sage-femme du service de PMA vous expliquera, lors de sa consultation, les modalités pratiques de ces injections et en particulier le fonctionnement du stylo auto-injecteur, pour que vous puissiez les réaliser vous-même ultérieurement.
En cas de nécessité, les infirmières des soins à domicile sont à votre disposition. N’hésitez pas à demander une ordonnance à votre gynécologue pour leurs visites à domicile.
Les médicaments sont disponibles sous forme de stylos («pens»), faciles à manipuler (PUREGON®, GONAL-F®), ou en seringues préremplies (ORGALUTRAN® 0,25 ; CETROTIDE® 0,25) ; pour d’autres il faut mélanger de la poudre (le médicament) avec du liquide (le solvant) avant de pouvoir l’injecter (MENOPUR®, FOSTIMON®, DECAPEPTYL® 0,1). Les aiguilles et seringues seront prescrites avec le médicament.
Les injections de DECAPEPTYL® 3,75 (1 ampoule entière ou ½ ampoule) et de PREGNYL® (1 ou 2 ampoules) se font dans le muscle (IM). Elles doivent obligatoirement être faites par une infirmière des soins à domicile. L’ordonnance pour l’infirmière vous est remise avec les prescriptions. Concernant l’injection de Pregnyl, elle doit être faite à une heure précise qui vous sera communiquée le jour-même.
Par précaution on jette les demi-ampoules non utilisées.
En pratique : Pour les injections intramusculaires vous devez faire appel aux services des soins à domicile qui se déplacent même le W-E et tard en soirée. Une liste des cabinets d’infirmiers est disponible au secrétariat du service PMA
Folliculométrie et prise de sang
Lors de la stimulation, il est indispensable de vérifier la croissance correcte des follicules ovariens par des échographies endovaginales (vessie vide) et des prises de sang successives (3-6 par cycle de stimulation). Lors de la prise de sang sont dosés l’oestradiol, la progestérone et la LH, dont les résultats sont confrontés à ceux de l’échographie.
Si vous réalisez ces examens chez votre gynécologue, il nous envoie par fax vos résultats avant midi (via un formulaire spécifique). Les résultats sont en effet évalués par l’équipe entre 12.00 et 13.00 heures.
À partir de 13.30 heures, vous contacterez la sagefemme coordinatrice pour qu’elle vous communique les consignes du médecin : vous saurez le jour du prochain contrôle et s’il y a lieu de changer la dose médicamenteuse (en unités), afin d’optimiser la réponse ovarienne.
Au fur et à mesure des échographies vous allez constater que les follicules augmentent de taille, et peut-être allez vous ressentir une légère pesanteur dans le bas-ventre. Ceci n’est pas inquiétant et s’explique tout simplement par le fait que les follicules en croissance occupent un certain volume. Un follicule mûr mesure entre 16 et 20 mm de diamètre moyen. Lors d’une hyperstimulation ovarienne contrôlée (FIV), chaque ovaire peut porter entre 5 et 12 follicules.
Lorsque la plupart des follicules ont atteint une taille correcte (vers le 11e-13e jour de stimulation), on vous dira d’arrêter les injections journalières et on vous communiquera l’heure exacte à laquelle vous devez recevoir l’injection de Pregnyl, qui déclenchera l’ovulation 36-40 heures plus tard.
5. Le prélèvement ovocytaire ou ponction folliculaire
La ponction folliculaire
Le jour de la ponction (le surlendemain de l’injection de PREGNYL), vous vous présentez à 06.00 heures, à jeun, au 2e étage de la maternité (secteur MAT 3). Veuillez vous munir de votre pièce d’identité qui vous sera demandée en secteur d’hospitalisation.
Vous serez ensuite conduite au bloc opératoire où sera réalisée la ponction folliculaire par un des gynécologues du service de PMA. Afin d’optimaliser l’organisation du service, chaque médecin a un jour fixe en semaine pour faire les ponctions.
Le type d’anesthésie administrée a été discuté au pré- alable en consultation avec votre gynécologue et/ou l’anesthésiste.
La ponction est réalisée par voie vaginale, sous contrôle échographique endovaginal.
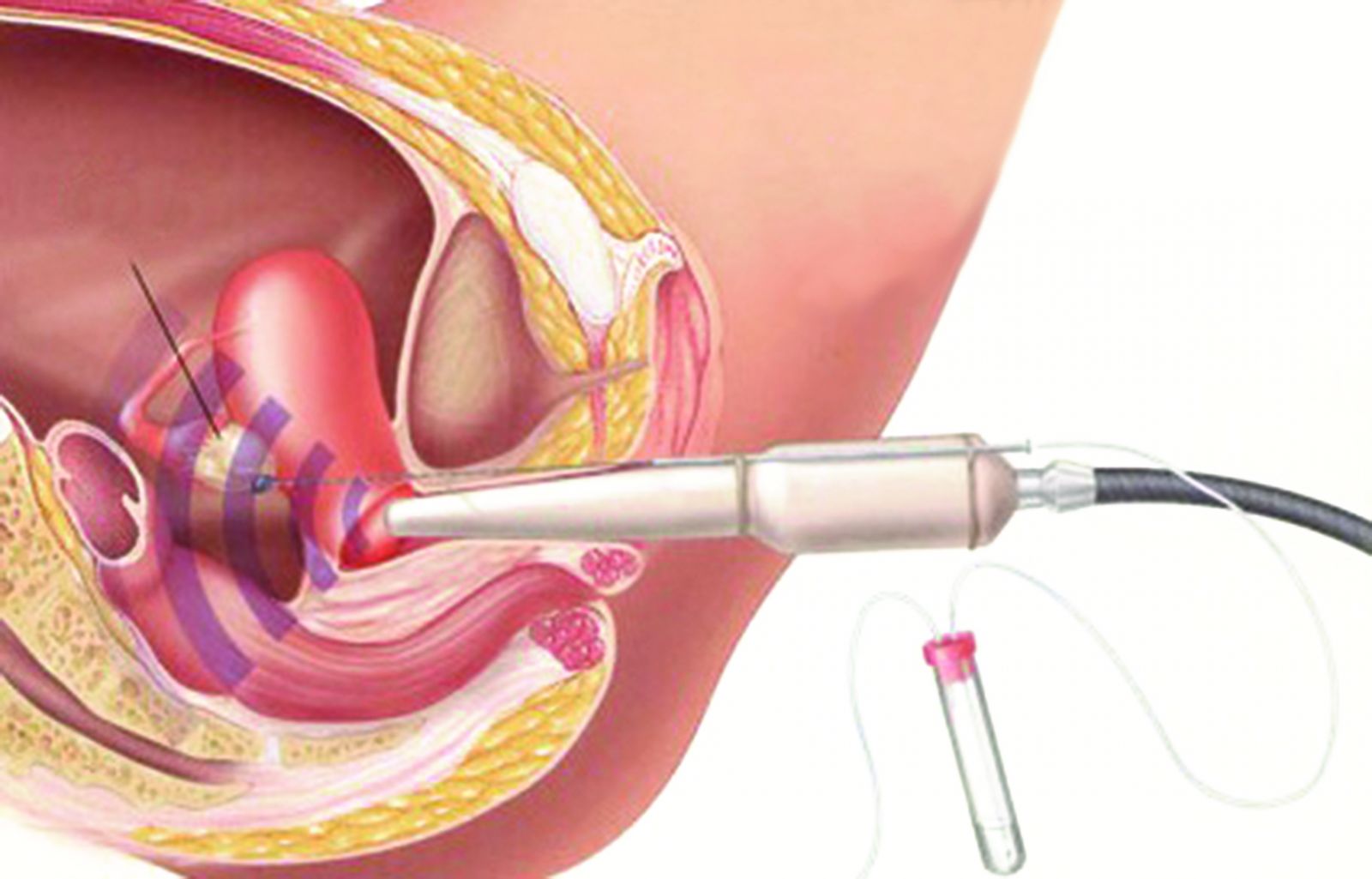
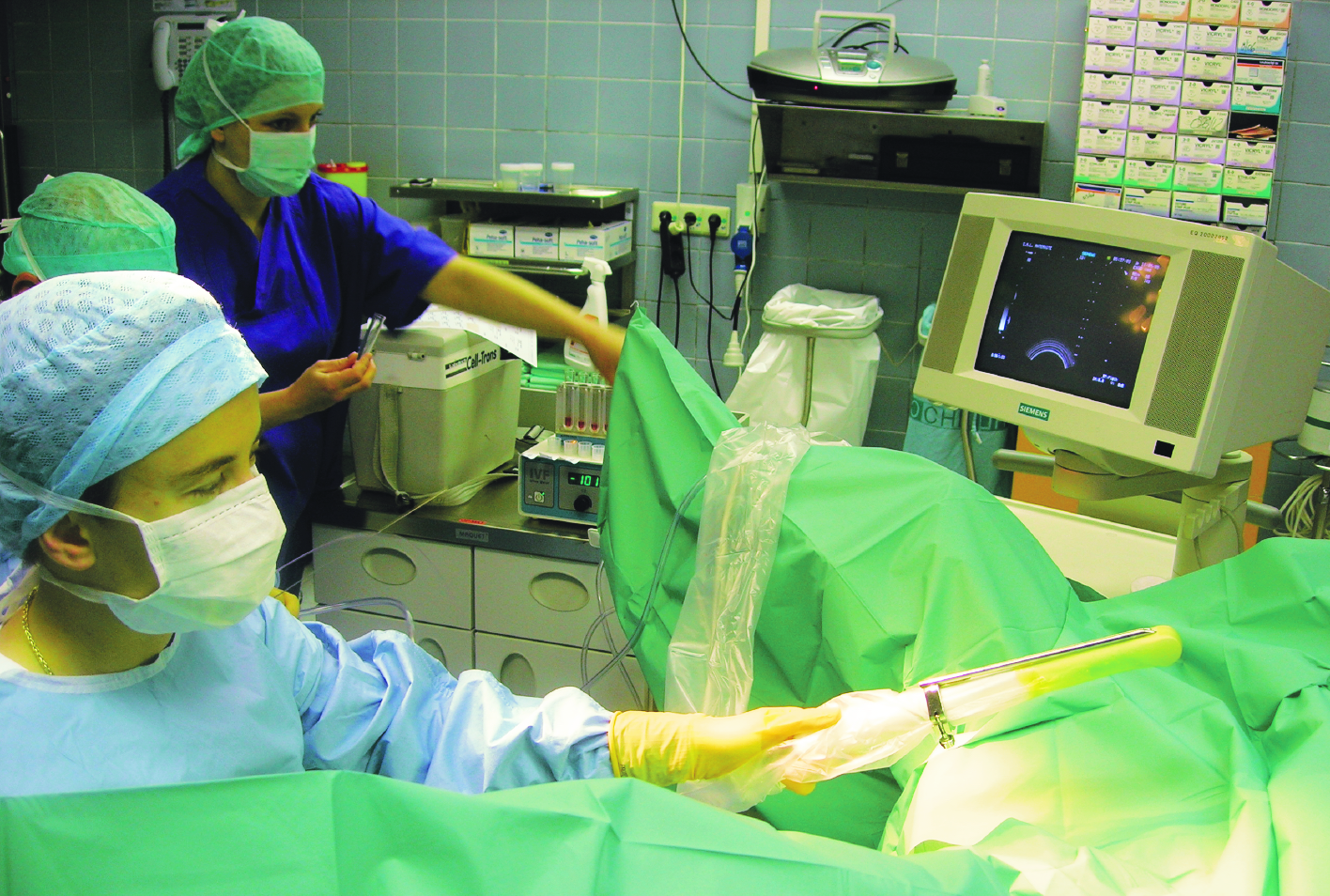
Gauche : Vue schématique de la ponction folliculaire. Droite : Ponction folliculaire au bloc opératoire de la Maternité G.-D. Charlotte.
Au cours de ce geste, l’aiguille de ponction traverse, sous contrôle de l’échographie, la paroi vaginale pour arriver dans le premier follicule, à la surface de l’ovaire. Le contenu du follicule, le liquide folliculaire est alors aspiré, et avec ce liquide, l’ovocyte est récupéré. L’aiguille est alors introduite dans le follicule suivant et ainsi, tous les follicules sont aspirés.
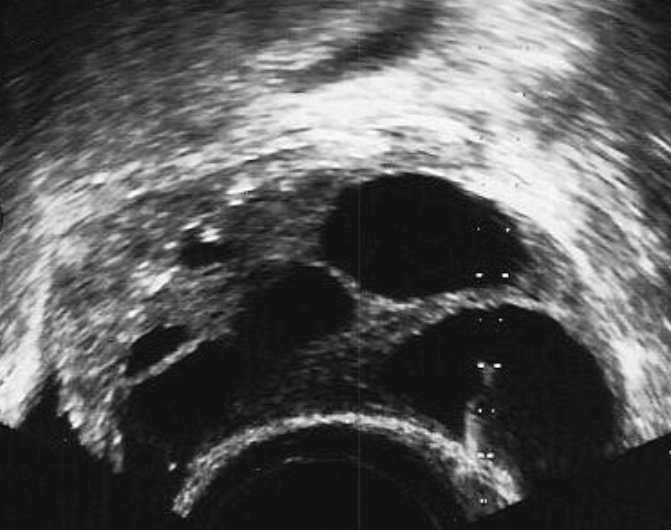
Image échographique d'un ovaire stimulé au moment de la ponction folliculaire
À la fin de l’intervention, les tubes contenant les liquides folliculaires et les ovocytes sont acheminés dans une boîte chauffante vers le laboratoire de PMA, où une technicienne de laboratoire les examinera sous une loupe, afin d’isoler les ovocytes. Elle retient les ovocytes de qualité suffisante afin de pouvoir réaliser une FIV voire une ICSI.
Il faut savoir que le plus souvent le nombre total d’ovocytes recueillis est inférieur à celui du nombre total de follicules comptés en échographie.
Pendant le temps de la ponction, votre conjoint réalise le recueil de sperme au laboratoire PMA.
En fin de matinée le médecin passera dans votre chambre pour vous communiquer le nombre d’ovocytes retenus et pour s’assurer qu’il n’y a pas de doléances en relation avec le geste de ponction.
Au besoin, vous allez recevoir un arrêt de maladie ainsi qu’une prescription de médicaments:
• De la Progestérone, Utrogestan®, afin de soutenir la deuxième phase du cycle qui risque d’être déficitaire dans le cadre d’une hyperstimulation ovarienne pour FIV/ICSI. L’administration se fait par voie vaginale, 3 fois par jour, jusqu’au test de grossesse.
Et éventuellement:
• Des antalgiques.
• Des antibiotiques à visée préventive, afin de diminuer les risques éventuels de la ponction.
Dans de rares cas, il se peut que l’on n’obtienne qu’un très petit nombre d’ovocytes voire aucun ovocyte à la ponction (ponction blanche). Ceci peut avoir diffé- rentes raisons qui seront discutées avec votre gynécologue.
Il faut savoir que dans ce cas, la tentative ne sera pas prise en compte par la Caisse de Santé.
6. Le travail au laboratoire
A la ponction, chaque ovocyte est entouré d’une enveloppe protéique, la zone pellucide (ZP), ainsi que d’une couche de cellules folliculaires formant le cumulus. L’ensemble est appelé le complexe cumulo-ovocytaire (CCO). Les CCO sont isolés des liquides folliculaires sous une loupe binoculaire, puis mis dans un milieu de culture. Comme indiqué plus haut, la fécondation peut être réalisée selon deux techniques.
FIV classique
Dans la technique de FIV classique, un nombre défini de spermatozoïdes préalablement préparés sont mis en contact avec les ovocytes dans une boîte du culture.
Le lendemain, à J1, soit environ 18 à 20 heures après la mise en culture, les CCO sont observés rapidement: une partie des cellules du cumulus s’est détachée spontanément de l’ovocyte. La dénudation de ces derniers est complétée mécaniquement et on peut alors observer la présence de signes de fécondation: 2 pronoyaux, 2 globules polaires.
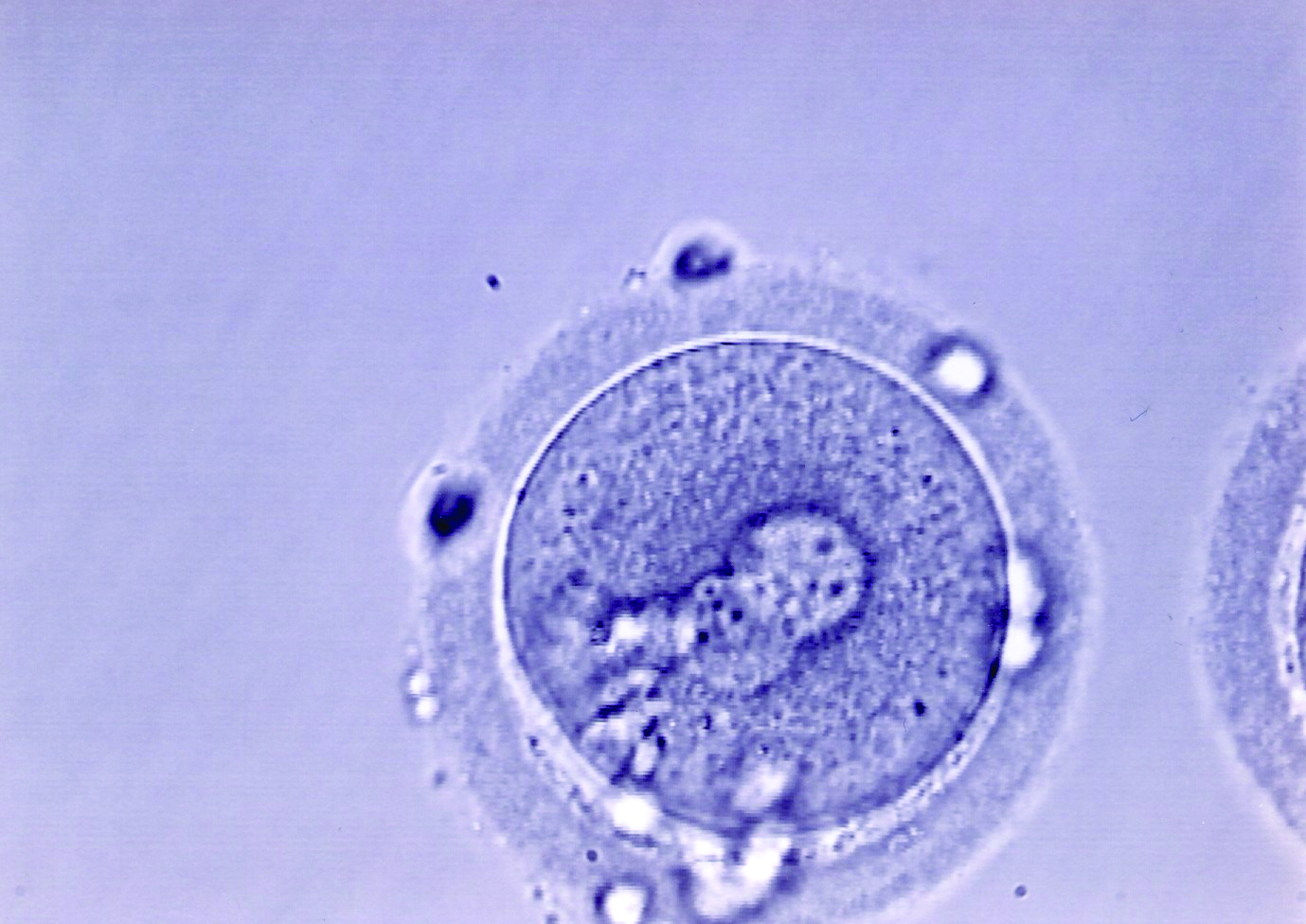
Ovocyte fécondé avec 2 pronoyaux et 2 globules polaires (=ZYGOTE)
Cette observation ne permet toutefois pas toujours de préjuger de l’évolution ultérieure, c’est pourquoi vous ne serez pas contactée par le laboratoire à J1.
Ce n’est donc qu’à J2 que le laboratoire vous appellera pour vous dire combien d’embryons se sont développés et de quelle qualité ils sont.
La notion de qualité est basée sur des critères morphologiques tels que le nombre de cellules (idéalement 4 à J2 et 8 à J3), la régularité des cellules (idéalement cellules de même taille), la visibilité d’un (seul) noyau, l’absence de fragments… etc.
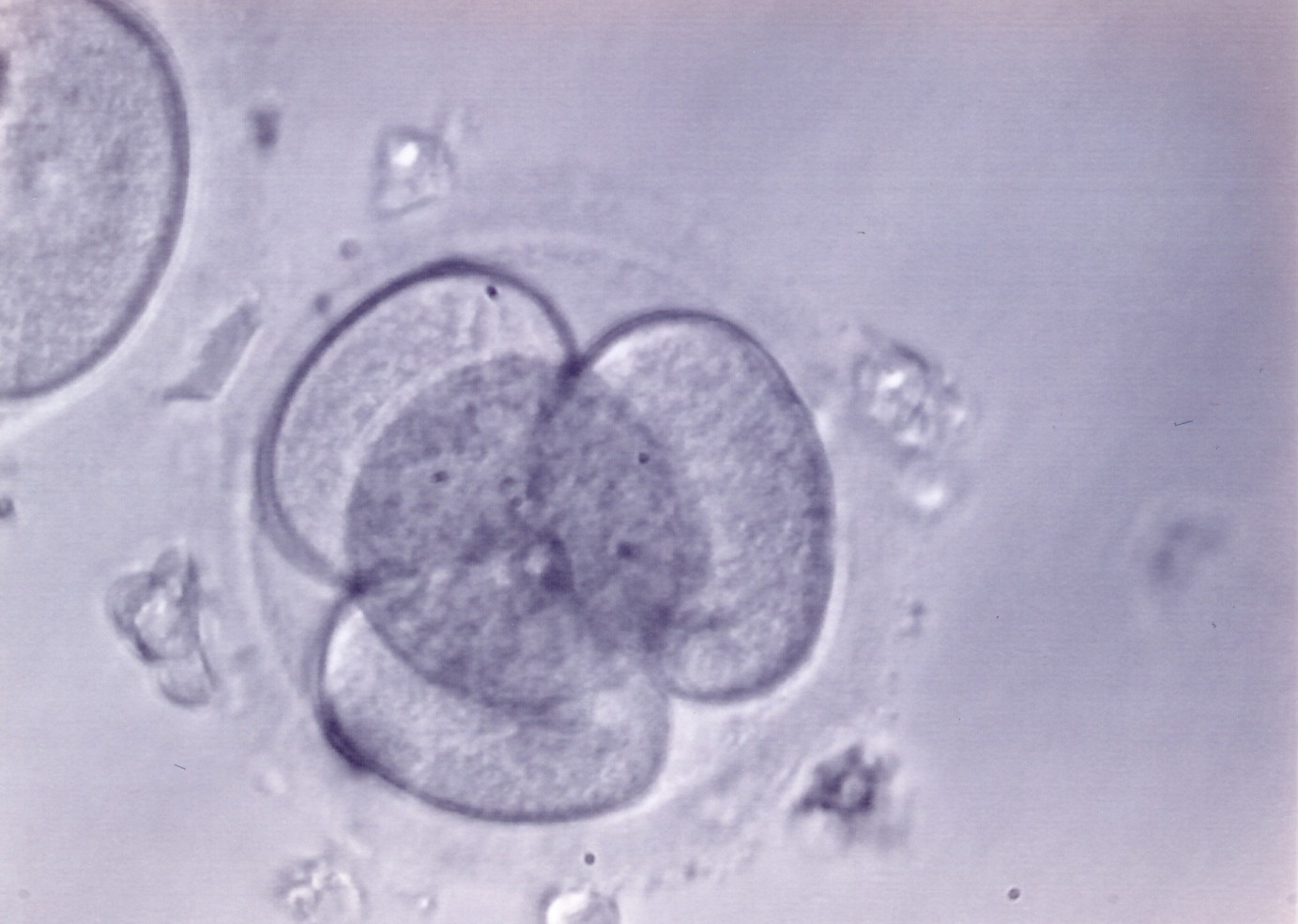
Embryon à 4 cellules
Le plus souvent, le transfert embryonnaire est fait au stade clivé, à J2 ou J3, et les embryons surnuméraires de bonne qualité sont congelés en vue d’un transfert ultérieur.
Dans certains cas, le transfert peut être retardé à J5 ou J6, au stade de blastocyste ; à ce moment on parlera de culture prolongée. (Figure 24).
Le transfert embryonnaire peut également être différé pour raisons médicales. Dans ce cas, tous les embryons, à condition toutefois d’avoir une qualité suffisante, sont congelés en vue d’un transfert ultérieur.
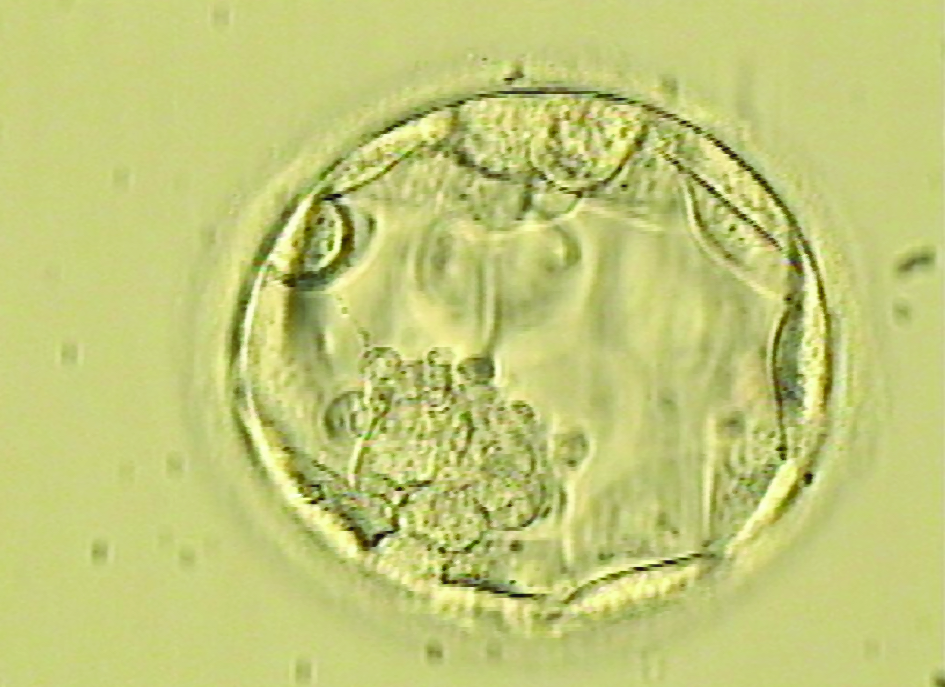
Embyron au stade blastocyte
FIV-ICSI (Intracytoplasmic Sperm Injection)
Contrairement à ce qui se passe en fécondation in vitro classique (voir page précédente), dans le cas d’une ICSI, les ovocytes recueillis à la ponction sont rapidement débarrassés du cumulus qui les entoure c’est l’étape de décoronisation. Une fois décoronisés, les ovocytes ne sont plus entourés que par leur zone pellucide et il est possible de voir un certain nombre de détails dont la présence ou non d’un globule polaire (figure 25). L’ovocyte a expulsé ce globule après le dernière injection du protocole de traitement (PREGNYL), afin de se séparer de la moitié de ses chromosomes. Ainsi, avec la moitié apportée par le spermatozoïde, le futur embryon sera doté d’un ensemble complet de chromosomes, pour moitié d'origine maternelle et pour moitié d’origine paternelle.
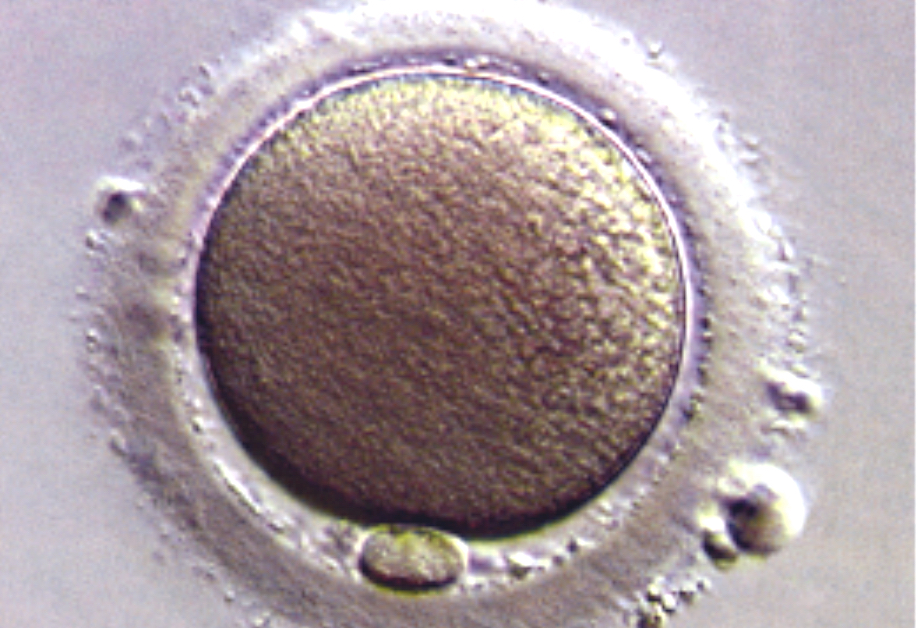
Ovocyte mature avec globule polaire
Autrement dit, seuls les ovocytes qui présentent ce globule polaire sont considérés comme étant matures et aptes à être fécondés; ceux qui ne présentent pas de globule polaire sont dits immatures et ne seront pas micro-injectés.
Les spermatozoïdes utilisés en ICSI doivent être vivants. Suivant les indications masculines, l’ICSI peut- être réalisée avec des spermatozoïdes éjaculés (frais ou congelés) ou prélevés chirurgicalement (par ponction épididymaire ou par biopsie testiculaire).
Après préparation selon différentes méthodes en fonction de l’origine du sperme, les spermatozoïdes sont placés dans une solution afin de les immobiliser. La micro-injection se fait sous le microscope équipé d’un micromanipulateur.
C’est une étape délicate qui consiste tenir d’un côté l’ovocyte avec une pipette de contention, et à injecter de l’autre côté un spermatozoïde avec une micro-aiguille.
Après la micro-injection, les ovocytes sont mis en culture comme pour une FIV classique et les autres étapes se déroulent de la même manière également.
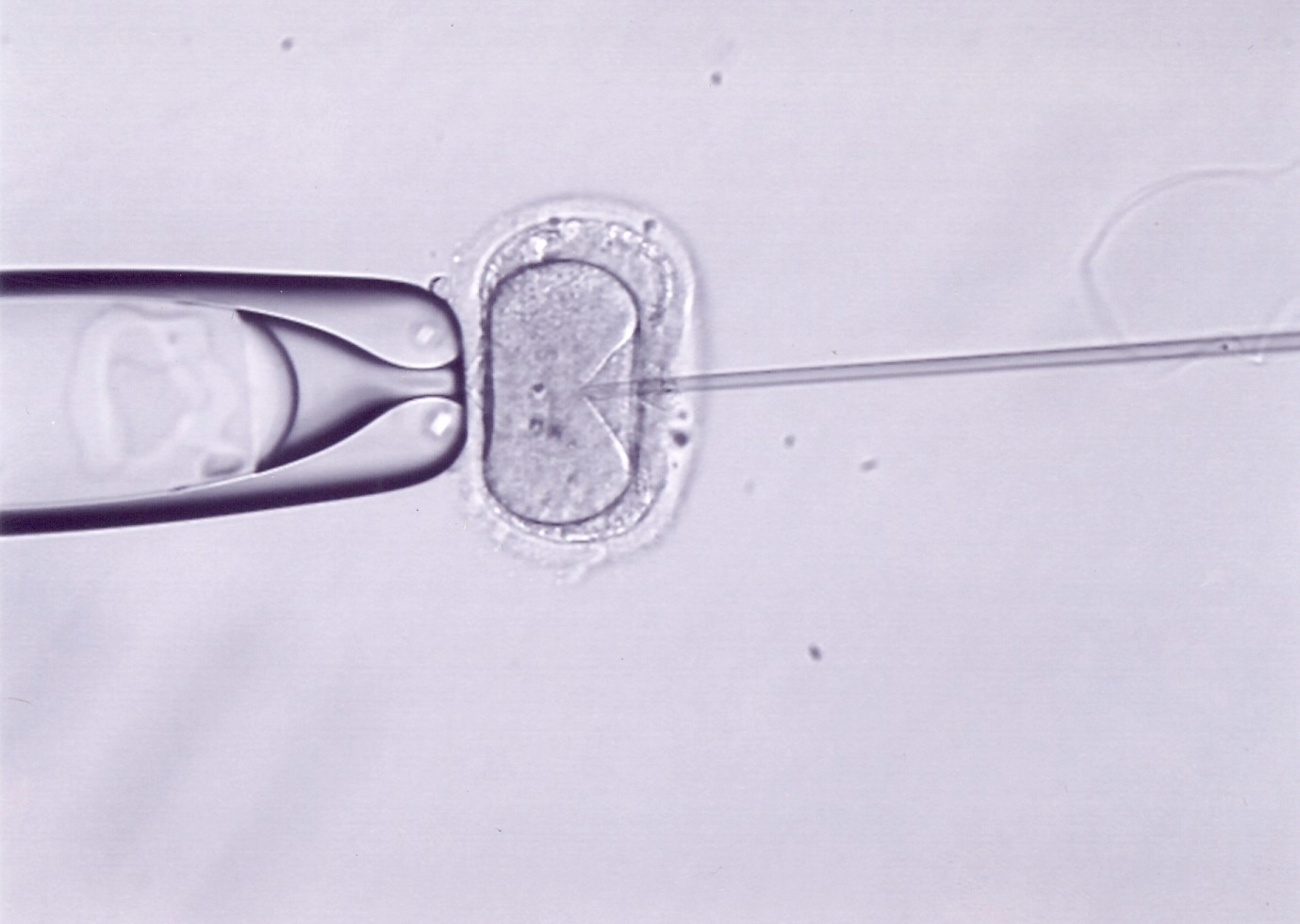
Intracytoplasmic sperm injection (ICSI)

Réalisation de l'ICSI
Éclosion assistée (Assisted hatching)
Préalablement au transfert on peut réaliser une éclosion assistée. Le principe consiste à fragiliser la zone pellucide, pour faciliter l’éclosion du blastocyste, à cet effet nous utilisons un rayon laser inoffensif pour l’embryon et permettant de faire des entailles dans la zone pellucide. Cette technique d’éclosion assistée est indiquée lorsque la pellucide est épaisse, en cas d’échecs implantatoires répétés et chez les patientes de plus de 37 ans à FSH élevée.
7. Le transfert embryonnaire
Le matin du transfert embryonnaire, la technicienne vous téléphone afin de vous communiquer le nombre total d’embryons obtenus et pour vous préciser l’heure à laquelle va avoir lieu le transfert.
La mise en place du ou des embryons dans l’utérus se fait après 2 ou 3 jours (stade clivé) ou plus rarement après 5 jours (stade blastocyste). Le nombre d’embryons à transférer est toujours décidé de commun accord avec le couple, le biologiste et le clinicien, et dépend principalement de l’âge de la patiente, mais aussi du nombre de tentatives réalisées auparavant, du nombre total d’embryons ainsi que de la qualité embryonnaire obtenue. Il ne peut toutefois dépasser deux embryons.
Afin d’optimiser l’organisation de l’activité du service, chaque médecin a un jour fixe dans la semaine pour faire les transferts.
Le geste du transfert est indolore et ne nécessite aucune anesthésie. Il est réalisé au 1er étage de la Maternité dans le service de PMA et consiste à introduire un fin cathéter souple à travers le col jusque dans la cavité utérine (figure 28). Le transfert est réalisé chez la patiente en position gynécologique sous contrôle échographique par voie abdominale, raison pour laquelle vous êtes priée de vous présenter avec la vessie remplie. De plus, une vessie remplie redresse l’utérus dans l’axe du corps et facilite l’introduction du cathéter.
Afin de rendre cette dernière étape le plus agréable et le moins stressant possible, vous avez la possibilité d’amener un CD de musique de votre choix.
Après le transfert la patiente peut rester allongée pendant quelques minutes, un repos plus prolongé étant inutile, car sans impact sur les chances de grossesse. Il faut en effet insister sur le fait que la cavité utérine est physiologiquement virtuelle et que l’embryon ne risque donc pas de «tomber» après le transfert.
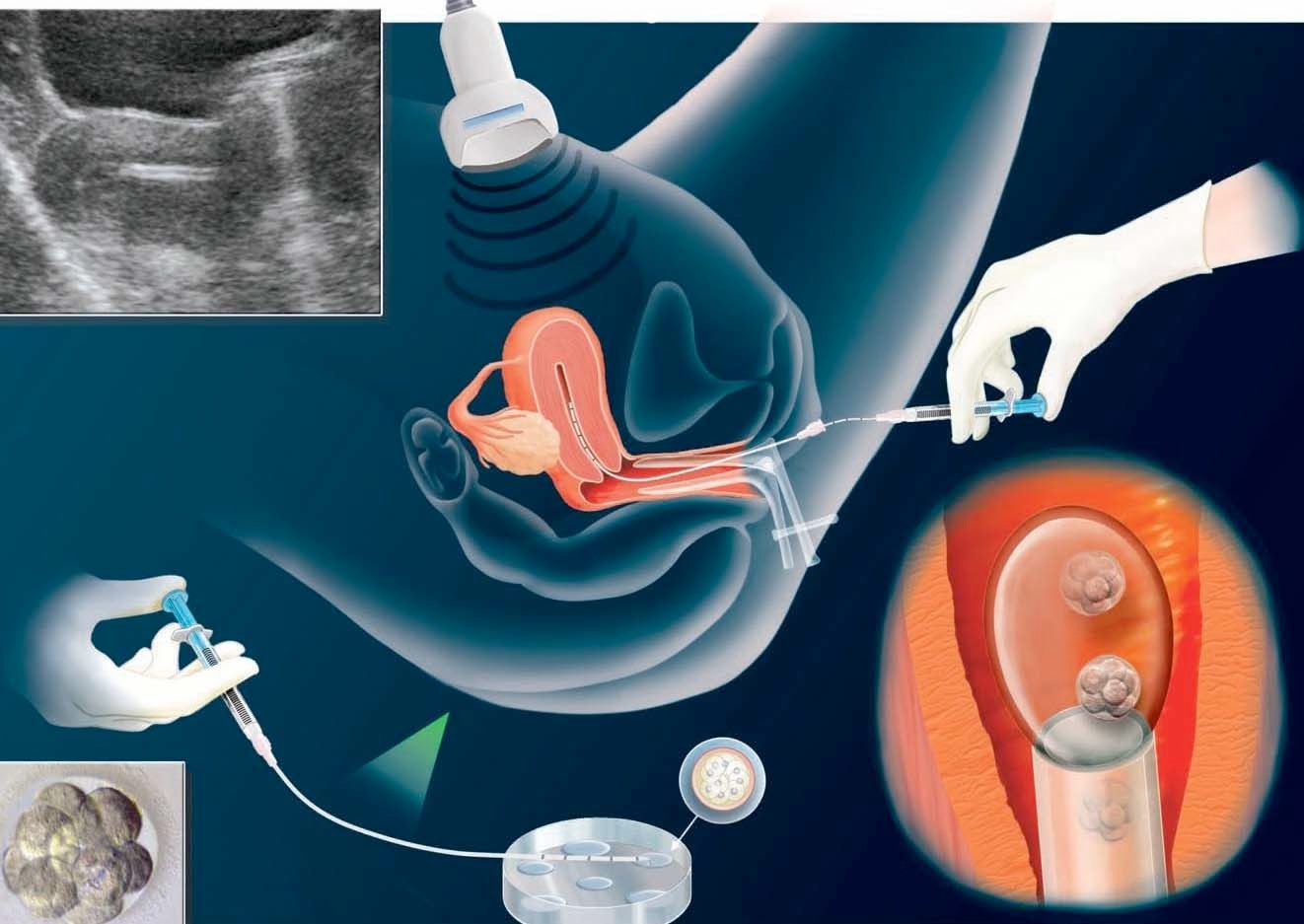
Déroulement du transfert embryonnaire
8. La congélation des embryons surnuméraires
Si plusieurs embryons de bonne qualité ont pu être obtenus lors de votre fécondation in vitro (FIV et/ou ICSI), nous avons la possibilité de congeler ces embryons surnuméraires. Pour cela, les embryons sont mélangés avec une substance qui les protège des effets du froid (cryoprotecteur), puis congelés selon la technique de vitrification et conservés dans l’azote liquide, à -196°C (figure 29). En pratique, cette conservation est prévue pour une durée d’un an au terme de laquelle vous pourrez prolonger cette conservation, ceci d’année en année, tant que vous aurez un projet parental pour ces embryons.
En cas d’absence de grossesse ou en cas de désir d’enfant après une grossesse réussie et une naissance, ce processus permet de vous transférer des embryons congelés sans devoir restimuler vos ovaires aux Gonadotrophines. Il suffit de préparer l’endomètre (muqueuse endo-utérine) à la nidation du ou des embryons transférés, au cours d’un cycle artificiel associant des oestrogènes naturels et de la progestérone naturelle. Dans certains cas, le transfert pourra être réalisé en cycle naturel.
Le suivi médical de la préparation endométriale est beaucoup moins rapproché que lors de la stimulation ovarienne: souvent sur RDV de contrôle (l’échographie et la prise de sang suffisent).
En pratique, le transfert d’embryon(s) congelé(s) (TEC) se déroule de la même façon que pour un transfert frais.
Le partenaire doit obligatoirement être présent au transfert d'embryon(s) congelé(s).
Il faut savoir que la probabilité de survie des embryons après décongélation (environ 80%) ainsi que le taux de grossesse dépendent surtout de leur qualité au moment de la congélation, raison pour laquelle nous ne congelons que les embryons de bonne qualité.
Enfin, la congélation en soi n’entraîne pas de surrisque pour la santé des enfants en termes de malformations ou d’anomalies chromosomiques.
Les congélations d’embryons requièrent le consentement du couple géniteur et les embryons sont conservés selon notre règlement interne pendant un an renouvelable sur demande des géniteurs jusqu’à l’âge de 45 ans pour la patiente. En cas d’abandon du projet parental, comme en cas de décès d’un des conjoints ou de séparation du couple, les embryons seront détruits.
9. Résumé du processus de FIV
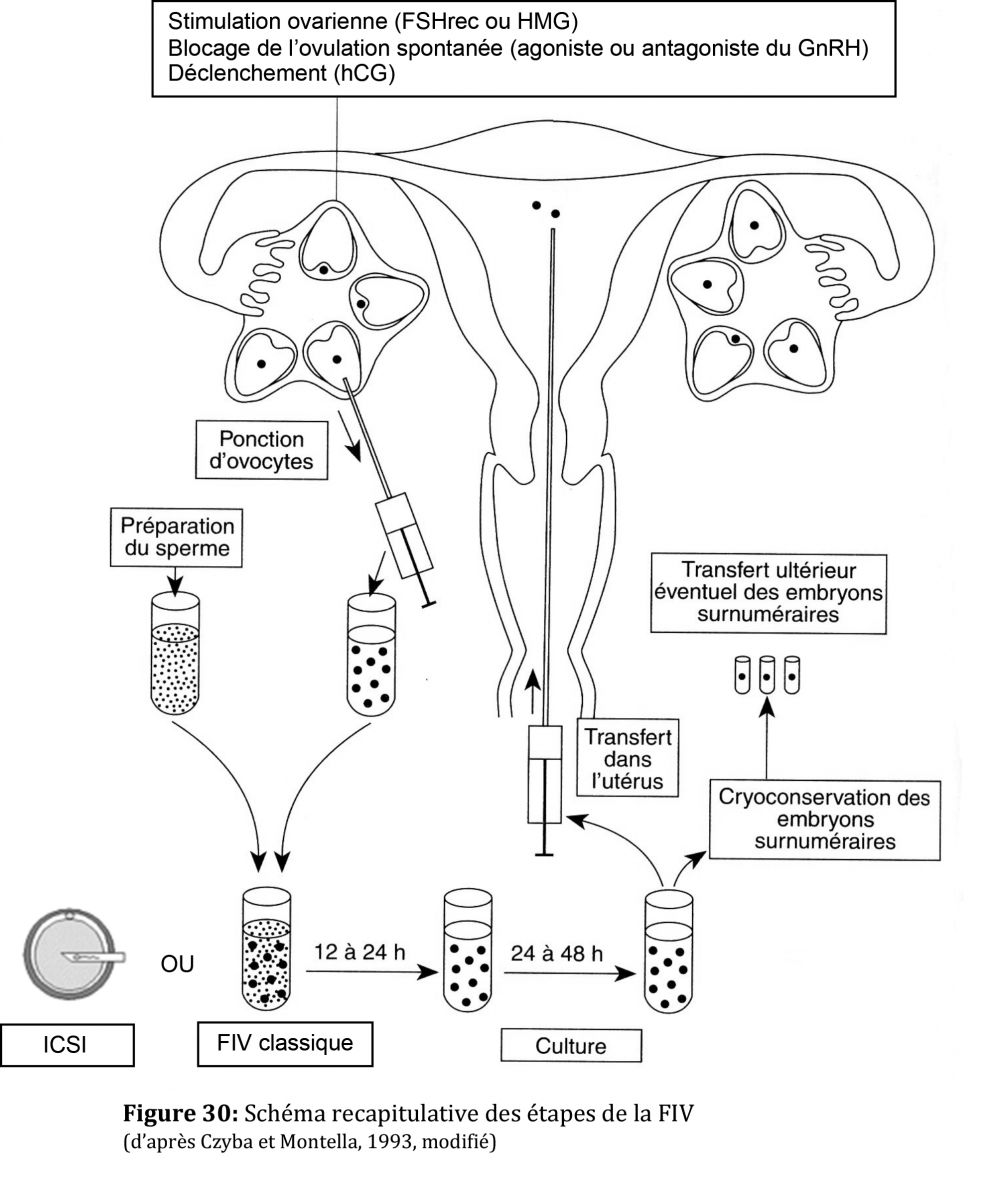
10. Le test de grossesse
Avant le test de grossesse
Un minimum de douze jours est nécessaire pour que le dosage sanguin de beta-hCG (test de grossesse) soit fiable.
Souvent, ces deux semaines d’attente entre le transfert embryonnaire et le test de grossesse sont vécues comme étant la période la plus difficile du traitement : en effet, cette attente qui échappe à tout contrôle aussi bien médical que personnel semble souvent très longue. Si vous le désirez, vous pouvez toujours appeler la sage-femme de PMA ou passer dans notre service.
Le test de grossesse
Le jour du transfert vous êtes prévenue du jour où vous allez réaliser le test de grossesse. Il est important de savoir qu’il faut faire la prise de sang même si vous êtes réglée. Il existe en effet des situations où une grossesse (éventuellement extrautérine) peut être en cours malgré des pertes de sang. Le jour de la prise de sang, vous êtes prévenue en début d’après-midi du résultat par la sage-femme de PMA.
Si votre test est positif, vous allez continuer la prise d’UTROGESTAN® et vous contrôlerez l’évolution du taux de β-hCG par une deuxième prise de sang une semaine plus tard. En cas de grossesse évolutive, l’augmentation est en effet exponentielle.
On parle de grossesse biochimique tant que l’on n’a pas de traduction échographique de la grossesse. Malheureusement, un certain nombre des grossesses biochimique ne vont pas évoluer en grossesses cliniques.
Dans le cas d’une grossesse clinique, une activité cardiaque peut être détectée à l’échographie à partir de 4 semaines après le transfert. Dans ce cas, vous allez prendre rendez-vous avec votre gynécologue traitant pour le suivi de la grossesse. Vous allez continuer l’UTROGESTAN® pendant 10 semaines environ.
Dans le cas d’un échec, vous pouvez arrêter l’UTROGESTAN® et reprendre un rendez-vous avec votre gynécologue du service PMA, afin de discuter des suites de la prise en charge.
11. Complications et problèmes techniques
Complications
Syndrome d’Hyperstimulation ovarienne (SHSO):
Réponse excessive des ovaires au traitement. Complication la plus fréquente (3% des patientes), surtout chez les femmes très jeunes et/ou avec ovaires micropolykystiques.
- Formes prévisibles: arrêt stimulation, parfois congé- lation de tous les embryons (pas de transfert frais).
- Formes non prévisibles: Survient dans les 8 à 10 jours après la FIV.
- Peut nécessiter une hospitalisation en raison de complications secondaires (rétention hydrosodée avec ascite, thromboses vasculaires…) parfois graves si elles ne sont pas prises en charge.
- N’empêche généralement pas l’évolution d’une grossesse.
Incidents d’anesthésie:
Une consultation auprès d’un médecin anesthésiste est obligatoire avant la ponction. En effet, si la ponction folliculaire est pratiquée sous anesthésie générale, les risques sont majorés chez les fumeuses, les patientes obèses ou porteuses d’allergies multiples.
Incidents liés à la ponction: rarissimes
- La blessure digestive: risque de péritonite
- La blessure vasculaire: risque d’hémorragie interne
- Complications infectieuses (abcès ovarien…)
Torsion d’ovaire hyperstimulé: très rare.
Urgence chirurgicale.
Grossesse extra-utérine (GEU):
Cette éventualité reste possible, même dans le cadre d’une FIV, car l’embryon ne s’implante pas immédiatement, mais reste à l’état libre pendant 2 à 3 jours et peut donc se déplacer dans l’utérus, s’engager dans une trompe et parfois ne plus en ressortir. Le traitement peut être chirurgical, parfois médicamenteux.
Grossesses multiples:
Gémellaires ou de haut rang ≥ 3. Ce risque dépend du nombre d’embryons réimplantés (Transfert de maximum 2 embryons à la fois dans notre centre). Une discussion des facteurs de risques avec l’équipe clinico-biologique doit limiter ces risques.
Malformations chez les enfants:
Les études internationales sont globalement rassurantes concernant les enfants issus de FIV ; néanmoins, dans la plupart des études, le taux d’anomalies est légèrement supérieur à celui de la population générale. Il n’y a pas de surrisque lié à la congélation.
Problèmes techniques
Réponse ovarienne insuffisante: peu de follicules à l’échographie, peu d’ovocytes, parfois aucun ovocyte à la ponction (= ponction blanche) Ce risque augmente avec l’âge
Immaturité ovocytaire: partielle ou totale (aucun ovocyte mature)
Paucifécondation: <50% des ovocytes matures injectés ou inséminés sont fécondés ; parfois échec de fé- condation (pas d’embryon du tout)
Transfert difficile: il arrive (très rarement) que le passage du col utérin soit moins aisé qu’attendu. L’utilisation d’un cathéter moins souple permet le plus souvent de contourner cette difficulté.
De façon exceptionnelle, il peut être nécessaire de ré- cupérer les embryons pour les congeler. A cette occasion, il peut arriver que les embryons ne soient pas retrouvés, notamment lorsque du sang est entré dans le cathéter.
Échec d’implantation: l’absence de grossesse après le transfert reste le problème le plus fréquent: s’il y a, en moyenne 30% de chances de succès pour une patiente jeune, il y a aussi 70% de risque d’échec.
Maturation In Vitro (MIV)
Il s’agit d’une alternative de traitement surtout chez les patientes avec des ovaires micropolykystiques et à haut risque d’hyperstimulation. Les ovaires ne sont quasiment pas stimulés et la ponction ovocytaire se fait délibérément à un moment où les ovocytes sont encore immatures. Ces ovocytes sont ensuite maturés au laboratoire, puis mis en fécondation in vitro.
Ce type de traitement est actuellement proposé par un petit nombre de centres à l’étranger et les chances de réussite sont inférieures à celles de la FIV/ICSI classique. Il a également sa place dans le cadre d’une préservation de la fertilité avant traitement potentiellement stérilisant, lorsque la stimulation hormonale est contre-indiquée.
Le diagnostic préimplantatoire (DIP)
Pour certains couples dont un des partenaires est porteur d’une maladie génétique grave, le fait d’avoir recours à un traitement par fécondation in vitro permet d’éviter la transmission de la maladie.
Il s’agit donc en général de couples qui au départ n’ont pas de problème d’infertilité.
Cette technique consiste à sélectionner les embryons qui ne sont pas porteurs de la maladie en question, en prélevant et en analysant une cellule de chaque embryon. Ne sont alors transférés que les embryons indemnes de la maladie génétique.
La technique du DPI n’est proposée que par quelques centres spécialisés en Belgique ou en France. Ainsi, notre rôle sera celui de coordinateur avec le centre à l’étranger afin de vous éviter au maximum les déplacements.
Don d'ovocytes
Les patientes qui ont une réserve ovarienne trop faible pour répondre correctement à la stimulation ovocytaire ou celles qui ont un risque de transmettre une maladie grave à l’enfant, peuvent avoir recours au don d’ovocytes, ce qui veut dire que les ovocytes d’une autre femme stimulée au préalable, vont être fécondés in vitro avec le sperme du conjoint de la patiente. Ensuite l’ (es) embryon(s) obtenu(s) vont être transféré(s) chez la patiente.
Ce traitement n’est actuellement pas proposé dans notre centre. Votre gynécologue peut vous renseigner sur les possibilités et les modalités dans différents pays.
Don d'embryons
Lorsque les deux membres du couple ont un risque de transmettre une maladie grave à l’enfant, ou lorsque les différentes tentatives de PMA intraconjugale n’ont pas permis d’obtenir d’embryons, il est possible d’envisager un don d’embryon.
Il s’agit concrètement d’un transfert d’embryon(s) congelé(s) qui proviennent d’un autre couple infertile ayant renoncé à la poursuite de son projet parental. Cette technique n’est pas encore disponible au Luxembourg et donc, si vous relevez de ce type de PMA, votre gynécologue vous orientera vers un centre à l’étranger, comme pour le don d’ovocytes.
Adoption/famille d'accueil
Pour toute information, vous pouvez vous adresser à: • Ministère de la Famille et de l’Intégration 12-14, avenue Emile Reuter L-919 Luxembourg Tél. +352 247-86532 ou +352 247-83692 • Maison de l’Adoption 10, cité Henry Dunant L-8095 Bertrange Tél. +352 2755-6442
Réglementations
Il faut savoir que les législations et réglementations en matière de médecine de la reproduction varient largement d’un pays à l’autre.
En général ce sont la Belgique et l’Espagne qui ont les réglementations les plus permissives.
L’Allemagne, l’Autriche, la Suisse et l’Italie ont les législations les plus restrictives.
